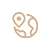科学家首次证实:LPS免疫调控衰老新机制,为皮肤细胞年轻化打开新大门!
LPS激活的巨噬细胞抑制细胞衰老并促进人皮肤成纤维细胞的年轻化
皮肤作为机体与环境之间的第一道屏障,不仅承受外源性氧化、感染和紫外线等持续胁迫,也面临内源性炎症、代谢紊乱及免疫细胞功能失调的累积打击。随着年龄增长,人皮肤成纤维细胞逐渐进入稳定的细胞周期停滞状态,并大量释放衰老相关分泌表型(SASP)因子,进一步放大局部炎症、降解细胞外基质,最终表现为皮肤变薄、弹性下降与修复能力衰退。传统抗衰老思路多聚焦于清除已形成的衰老细胞或抑制SASP信号,然而对"如何逆转衰老表型、恢复细胞功能"仍缺乏直接证据与可行策略。
组织驻留巨噬细胞因其可塑性强、分泌谱广泛,被视为调控皮肤稳态与修复的关键"指挥塔"。既往研究普遍认为,巨噬细胞在模式识别受体(如Toll样受体4)激动剂——脂多糖(LPS)刺激下主要向促炎M1表型极化,可能加速氧化损伤与细胞衰老。然而我们前期口服低剂量LPS的研究却意外发现,其可在不诱发全身炎症的前提下显著提升腹腔巨噬细胞及脑小胶质细胞的吞噬与抗炎功能,并改善多种衰老相关病理指标。这提示"LPS-巨噬细胞"轴的作用远比"促炎促衰"更为复杂,亦可能通过分泌活性分子直接干预成纤维细胞的命运决定。
基于此,本研究首次系统评估了LPS激活的人巨噬细胞条件培养基(THP/LPS-CM)对皮肤成纤维细胞衰老与年轻化的双向影响。通过构建"年轻-衰老"共培养模型,结合P16、P21与Ki-67等多层次衰老标志分析,我们旨在阐明:
1.巨噬细胞源性可溶性因子能否阻断SASP诱导的继发性衰老;
2.已建立的衰老表型是否可被逆转并恢复增殖潜能。
该发现不仅有望刷新"LPS即促衰"的传统认知,也为皮肤乃至系统性衰老的免疫-分泌调控提供新的理论与干预思路。
LPS激活的巨噬细胞抑制细胞衰老并促进人皮肤成纤维细胞的年轻化
摘要
组织驻留巨噬细胞对维持皮肤稳态至关重要。本研究探讨了脂多糖(LPS)激活的巨噬细胞是否会影响人皮肤成纤维细胞的衰老与年轻化。实验通过使用源自成团泛菌的LPS泛菌糖脂质(1-1000 ng/mL)刺激人单核细胞THP-1,并收集其培养上清液。这些上清液被应用于两组NB1RGB成纤维细胞群体:一组为年轻活跃的分裂细胞(Young细胞),另一组为具有高倍增率但增殖能力减退的衰老细胞(Old细胞)。在基因和蛋白质水平分析了衰老标志物P16、P21和Ki-67的表达情况。实验结果显示,Old细胞的条件培养基可诱导 Young细胞衰老,表现为P16和P21表达水平升高。该衰老效应可被LPS激活的THP-1上清液联合处理所抑制。经LPS激活上清液处理的Old细胞则表现出P16和P21水平下降,同时Ki-67表达增加,表明其实现了部分细胞年轻化。这些效应在未刺激的THP-1上清液或单独使用LPS处理组中均未观察到。综上所述,本研究证实LPS激活的巨噬细胞分泌因子能够抑制细胞衰老并促进人皮肤成纤维细胞的年轻化,突显了巨噬细胞激活在调控细胞衰老中的潜在作用,为皮肤衰老干预提供了有前景的新策略。
关键词:衰老;老化;年轻化;LPS;巨噬细胞;成纤维细胞
引言
正常体细胞会暴露于多种应激源,包括炎症诱导的氧化应激和溶酶体功能障碍,这些因素会导致端粒缩短和基因组DNA损伤,最终引发不可逆的细胞周期停滞和增殖能力丧失[1]。当细胞达到复制极限时,通常会进入G1期停滞并走向凋亡[2,3]。然而,病理性衰老细胞常对凋亡产生抗性,即便处于生长停滞状态仍能在组织中持续存在[4]。这些细胞会分泌一系列被称为衰老相关分泌表型(SASP)的促炎因子,包括细胞因子[5]、趋化因子[6]、基质降解酶[7]、生长因子以及外泌体中的DNA片段[8]。SASP成分不仅导致慢性炎症性疾病,还会在邻近健康细胞中诱导类似衰老的特征,例如细胞周期停滞和凋亡抵抗[9,10]。
前景可期的抗衰老策略包括:抑制SASP诱导的继发性衰老、有效清除衰老细胞以及使衰老细胞恢复功能(即年轻化)[11]。
病理性衰老细胞通常通过表达免疫检查点分子(如PD-L1)来逃避免疫清除,这些分子会抑制免疫细胞功能。使用抗PD-1抗体恢复免疫监视的疗法,已显示出清除衰老细胞的潜力[12–14]。然而,目前很少有研究聚焦于逆转细胞衰老并促进其年轻化。本研究旨在同时解决SASP诱导的衰老预防和衰老细胞年轻化这两个关键问题。
具体而言,我们重点关注先天免疫系统(尤其是巨噬细胞)的抗衰老潜力。这些细胞在应对病原体时会产生活性氧和促炎细胞因子,从而加剧与衰老相关的炎症反应[15]。相反,组织驻留型巨噬细胞则通过调节炎症并支持组织修复发挥作用[16],这凸显了其在衰老过程中的双重角色[17]。然而研究表明,它们的吞噬能力随年龄增长而下降[18],这可能与年龄相关的微环境变化有关。因此,靶向激活巨噬细胞或许能提供一种不同于传统吞噬清除衰老细胞策略的新型抗衰老方案。这种新方法通过预防细胞衰老并促进细胞年轻化,这意味着通过外部刺激激活巨噬细胞,可能成为实现抗衰老的有效策略。
我们此前研究已证实,口服脂多糖(LPS)能安全有效地增强巨噬细胞的吞噬功能[19,20]。尽管体外实验或注射LPS具有促炎作用,但口服给药不会引发全身性炎症反应,反而能激活腹腔和脑部巨噬细胞(小胶质细胞)的吞噬活性。此外,口服LPS可降低氧化应激和炎症标志物水平,提升抗炎及组织修复相关指标,并改善阿尔茨海默病、糖尿病性脑病、动脉粥样硬化(ApoE缺陷小鼠)和2型糖尿病(肥胖KK-Ay小鼠模型)等衰老相关疾病模型中的不良影响[19,20]。这些发现表明,LPS能增强巨噬细胞的修复与抗炎功能,从而改善衰老相关病理。然而,LPS激活是否能逆转成纤维细胞的功能衰退尚不明确。因此,本研究旨在探讨LPS激活的巨噬细胞是否能抑制人皮肤成纤维细胞的衰老并促进其年轻化。
基于上述研究背景,我们提出假设:LPS激活的组织驻留巨噬细胞不仅能通过吞噬作用清除衰老细胞,还可能通过抑制细胞衰老进程并促进细胞年轻化,从而发挥抗衰老作用。为验证此假设,,我们评估了LPS刺激巨噬细胞条件培养基对人皮肤成纤维细胞的影响。实验将NB1RGB成纤维细胞分为年轻组与衰老组,并检测其衰老相关标志物P16、P21和Ki-67的表达水平。研究发现,衰老成纤维细胞的培养上清可诱导年轻细胞出现类似衰老的表型,而联合使用LPS刺激的巨噬细胞条件培养基则能有效抑制该诱导效应。此外,用该条件培养基处理衰老成纤维细胞后,P16和P21表达水平下降,同时Ki-67水平升高,表明细胞呈现年轻化特征。这些发现表明,靶向激活巨噬细胞可能成为预防细胞衰老、促进细胞年轻化的新策略,这为抗衰老研究开辟了区别于传统抗衰老策略的新途径。
结果
LPS刺激的巨噬细胞条件培养基对P16和P21表达的抑制作用
巨噬细胞的抗衰老潜力可从抑制衰老和促进年轻化两个角度进行评估。为验证其对衰老的抑制作用,我们采用既往研究报道的实验体系[21]——通过衰老细胞释放的SASP因子诱导年轻细胞产生衰老表型。总体而言,在经衰老成纤维细胞条件培养基处理的年轻NB1RGB细胞中,LPS激活的THP-1细胞条件培养基能显著抑制衰老标志物P16和P21的表达。相比之下,未刺激THP-1细胞的条件培养基则未呈现此种效应。这些结果表明,LPS激活的巨噬细胞通过分泌特定因子,能够有效抵抗SASP诱导的年轻成纤维细胞衰老(图1A,图1D)。
图1.Young细胞中p16和p21基因的表达。
由于人皮肤成纤维细胞(NB1RGB)与THP-1巨噬细胞样细胞分别使用Eagle最低必需培养基(EMEM)和 RPMI-1640 培养基培养,共培养时采用两种培养基1:1混合。初步试验证实,该混合物不会改变细胞行为。
我们研究了经LPS刺激的THP-1细胞条件培养基(THP/LPS-CM;0–1000 ng/mL)能否抑制高群体倍增数(PDL 53.9–67.9)、增殖力下降的衰老 NB1RGB 成纤维细胞(Old 细胞)条件培养基(Old CM)对年轻 NB1RGB 细胞(Young 细胞;PDL 14.9–22.9)的促衰作用。当将Old CM加入Young细胞后,细胞周期蛋白依赖性激酶抑制剂及经典衰老标志物P16与 P21的mRNA和蛋白表达水平均显著升高(图 1A,B)。当将Old CM与未经LPS刺激的THP/LPS (0 ng/mL)-CM混合时也观察到类似增加,证实了未经LPS刺激的THP-1上清液不能阻断SASP诱导的衰老。然而,添加THP/LPS(10-1000 ng/mL)-CM后,P16和P21表达水平显著降低至接近未处理Young细胞的基线水平。
为验证这些蛋白质水平的影响,我们进行了蛋白质印迹实验(图1C,D)。尽管P16蛋白的表达水平过低,难以可靠检测(图1C),但在使用Old CM–THP/LPS(0 ng/mL)-CM混合物处理的Young细胞中,P21蛋白表达显著升高,而在使用THP/LPS(10或100 ng/mL)-CM处理的细胞中则显著降低(图1D)。这些结果表明,LPS激活的巨噬细胞分泌的因子,能够中和SASP诱导的年轻成纤维细胞衰老。
THP/LPS条件培养基对衰老细胞的年轻化作用
鉴于THP/LPS-CM能抑制Young细胞的衰老诱导,我们进一步探究其是否能逆转Old细胞衰老的能力。具体而言,我们分析了经THP/LPS-CM处理的衰老NB1RGB细胞中p16、p21及增殖标志物Ki-67 [23]的mRNA表达水平。值得注意的是,用THP/LPS条件培养基(THP/LPS-CM)处理衰老NB1RGB成纤维细胞(Old细胞)后,衰老标志物p16和p21的表达显著降低,而增殖标志物Ki-67的表达则明显升高。然而,在未受刺激的THP-1细胞条件培养基或直接LPS处理的细胞中,均未观察到这些变化。因此,表明LPS激活巨噬细胞分泌的因子可能部分逆转衰老表型并促进细胞年轻化(图2A-D)。
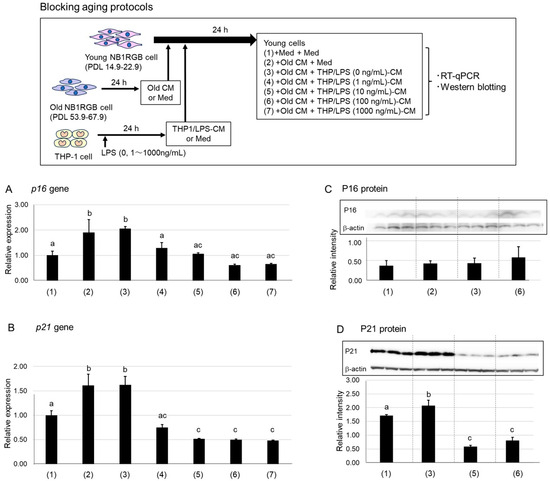
图2.经THP/LPSCM处理的衰老NB1RGB细胞中P16、P21和Ki-67表达的变化。
与年轻细胞相比,老年细胞的p16 和 p21水平显著升高,而 Ki-67 水平显著降低,证实了其衰老表型(图 2A)。相反,THP/LPS(0 ng/mL)-CM处理未产生此类效应。然而,用THP/LPS(10–100 ng/mL)-CM 处理显著降低了p16和p21的表达水平,同时提高了Ki-67水平,表明衰老表型得到部分逆转。值得注意的是,单独用LPS(10-1000 ng/mL)直接处理老年细胞并未改变p16、p21或Ki-67的表达,这表明LPS本身不会直接影响衰老的成纤维细胞(图2B)。
为进一步评估蛋白质表达和细胞定位,我们进行了核蛋白P21和Ki-67的免疫荧光染色(图2C),并同步完成细胞核与肌动蛋白染色。P16水平仍过低无法分析;P21和Ki-67的核定位得到证实。在Young细胞和经THP/LPS(100 ng/mL)-CM处理的老细胞中,P21染色较弱,而Ki-67染色较强。相反,未处理的老细胞和THP/LPS(0 ng/mL)-CM处理的细胞呈现强P21和弱Ki-67信号。在细胞中没有观察到明显的形态学变化。
阳性细胞的定量分析和每个视野的总细胞计数见图2D。与未处理组和THP/LPS(0 ng/mL)条件培养基处理的衰老细胞相比,Young细胞和经THP/LPS(100 ng/mL)-CM处理的衰老细胞中P21阳性细胞显著减少,而Ki-67阳性细胞数量明显增加。此外,Young细胞和THP/LPS (100 ng/mL)-CM处理的老细胞中每个视野的细胞数量也显著更高。
综上所述,这些研究结果表明:THP/LPS-CM条件培养基处理能够改变衰老成纤维细胞中衰老相关标志物与增殖相关标志物的表达,使其表型向年轻细胞转变,从而证实该处理具有促进细胞年轻化的作用。
讨论
本研究初步评估了LPS激活的巨噬细胞预防和逆转人皮肤成纤维细胞(NB1RGB)衰老的能力。实验采用已在细胞衰老研究中得到验证的衰老标志物P16、P21和Ki-67,来评估细胞的衰老与年轻化表型。
当在年轻细胞中加入衰老细胞条件培养基时,p16和p21表达水平显著升高,证实了SASP诱导细胞衰老(图1)。值得注意的是,与THP/LPS-CM联合处理可抑制这种表型。而未受刺激的THP-1细胞来源的CM则未表现出此效应,表明LPS激活是诱导保护性因子的必要条件。这些结果表明,LPS刺激的巨噬细胞可分泌对抗SASP介导衰老的分子。这一发现出乎意料。既往研究主要将巨噬细胞的抗衰老作用归因于其对衰老细胞的吞噬清除。而本研究首次提出证据表明,巨噬细胞还可通过可溶性因子发挥抗衰老作用,且该作用不依赖于吞噬作用。总体而言,这些发现揭示了一种先前未被认识的机制,即巨噬细胞可能通过分泌活性分子促进细胞年轻化。
本研究选用THP-1细胞作为巨噬细胞谱系的代表性模型。在体内环境中,巨噬细胞主要由组织驻留型巨噬细胞构成,这类细胞具有高度异质性,能适应不同组织微环境。尽管目前已有源自肺泡、肠道及脑组织巨噬细胞的多种细胞系,但至今仍未出现能普遍准确代表组织驻留型巨噬细胞的通用细胞系。但至今仍未出现能被普遍认可、能准确代表组织驻留型巨噬细胞的通用细胞系。
根据我们的实验观察,未分化的THP-1细胞对LPS的反应水平与肺泡、腹腔及小胶质巨噬细胞相似。因此,本研究选择未经TPA刺激的THP-1细胞作为模型系统,该选择也得到既往研究文献[24,25]的支持。相比之下,TPA诱导分化的THP-1细胞对LPS的反应过于剧烈,可能不适合作为组织驻留巨噬细胞表型的通用模型。基于此,我们最终选定未分化的THP-1细胞作为巨噬细胞模型,该模型能够展现类似组织驻留细胞的特征,尤其在LPS诱导的先天免疫激活方面具有典型性。
随后我们通过直接处理衰老细胞,验证THP/LPS条件培养基能否逆转已建立的衰老状态(图2)。出乎意料的是,该处理显著降低了p16和p21的基因表达水平,同时提升了Ki-67的表达。免疫荧光显微镜观察进一步显示P21阳性细胞减少而Ki-67阳性细胞增加。每个视野中增加的细胞数量表明增殖能力得到部分恢复,这提示细胞年轻化现象的发生,但未观察到明显的细胞形态学差异。值得注意的是,单独使用LPS直接处理并不能复制这种效应,从而印证了巨噬细胞源因子在年轻化过程中的关键作用。尽管本研究仅分析了三种经典标志物,但这些发现为理解巨噬细胞参与衰老过程的机制提供了新的视角。
在本研究中,我们清晰明确观察到p16基因表达的变化,但P16蛋白水平因表达量过低而难以准确检测。由于目前缺乏关于NB1RGB细胞中P16表达水平的相关参考数据,该细胞系可能仅以极低水平表达该蛋白。未来研究应通过RNAscope技术定量CDKN2A mRNA来解决这一问题。此外,后续实验还应补充 LMNB1 和 γH2AX 等互补标志物,以完善评估体系进一步验证结果。
经低浓度LPS刺激的巨噬细胞培养上清液中,具体哪些年轻化因子发挥作用尚待明确。据文献报道,IL-4、IL-10及TGF-β等2型炎症抑制因子可能是潜在候选因子[26]。总体而言,衰老过程伴随低度慢性炎症(即炎症衰老),这种状态会促进多种年龄相关疾病的发生。IL-4和IL-10能抑制单核/巨噬细胞及其他免疫细胞分泌TNF-α、IL-6、IL-1β等促炎细胞因子,同时还可抑制NF-κB信号通路——该通路是年龄相关炎症的关键调控途径。因此,IL-4与IL-10既能减轻全身性炎症,又有助于保护组织免受慢性免疫介导的损伤。此外,这些细胞因子还能抑制衰老巨噬细胞中SASP因子的产生,从而减少组织损伤。既往研究也报道了在某些实验条件下,细胞衰老标志物P16和P21的表达会因这些因子而下调。综合现有证据表明,IL-4和IL-10是巨噬细胞响应LPS刺激后可能产生的关键候选细胞因子。
从作用机制来看,TGF-β会促进P16和P21的表达,从而加速衰老进程。TGF-β信号通过激活SMAD通路,可能诱导这两种参与细胞周期阻滞的蛋白表达[27]。此外,TGF-β作为SASP网络的关键成员,还能进一步强化细胞退出周期的进程。通常LPS通过Toll样受体4激活巨噬细胞,促使其分化为M1型(促炎型)巨噬细胞。在体外实验或小鼠模型研究表明,LPS刺激会抑制巨噬细胞中TGF-β mRNA的表达[28]。并阻断下游 SMAD 通路的激活,从而在炎症环境中削弱 TGF-β 信号。因此,不能排除 LPS 激活巨噬细胞通过“抑制 TGF-β”这一机制来延缓衰老的可能性。未来我们将进一步重点研究,抗炎因子是否通过抑制衰老细胞产生SASP或调控P16/P21蛋白的诱导来发挥作用。
巨噬细胞通过可溶性因子和趋化作用与组织驻留巨噬细胞进行信息交流。我们此前提出的“巨噬细胞网络”概念表明,被激活的巨噬细胞不仅调控局部炎症和组织修复,还能调节维持全身稳态[19,20]。例如,口服 LPS 可提升外周白细胞膜结合型集落刺激因子 1(CSF1)的水平,进而激活小胶质细胞上的CSF1受体,发挥神经保护作用[29]。这一发现支持了LPS能诱导M2样(抗炎)巨噬细胞表型的假设,这种表型可能有助于延缓衰老进程并促进组织更新。
本研究采用低剂量LPS激活的巨噬细胞上清液构建体外模型,用于检测其对成纤维细胞的间接作用[25,30]。据此,我们评估了巨噬细胞源性因子在细胞衰老中的预防与修复特性。组织驻留巨噬细胞作为免疫监视、组织修复与再生的关键执行者,其功能会因组织来源和激活状态而异。例如,在骨重塑中,破骨细胞(特化的巨噬细胞)与成骨细胞相互作用以维持骨骼稳态 [31]。巨噬细胞大致分为促炎性M1和抗炎性/再生性M2两种亚型。在皮肤中,M1型巨噬细胞随年龄增长而累积,而M2型则更常见于年轻组织中[17]。此外,衰老会削弱皮肤巨噬细胞的吞噬功能与抗炎能力[32],这种功能障碍在慢性肾病等疾病状态中亦有体现[33]。这些发现凸显了维持巨噬细胞功能平衡对组织稳态与年轻态的重要性。已有研究显示,局部涂抹Pantoea agglomerans来源的LPS可逆转小鼠与年龄相关的表皮变薄 [34],该发现与本研究中LPS激活的巨噬细胞能够使人衰老成纤维细胞重现年轻化特征的结果相互印证。
尽管LPS因其能引发活性氧(ROS)和促炎细胞因子的产生而常被认为具有促衰老作用[35],但这些效应通常源于疾病模型中的全身注射[36]。相反,来自黏膜表面(如皮肤、肠道和呼吸道)共生革兰氏阴性菌的低剂量LPS可产生抗炎和修复性反应。口服或局部低剂量LPS在糖尿病、动脉粥样硬化、痴呆和过敏性皮炎模型中已显示出益处[19,20]。模拟口服LPS暴露的体外实验模型也表明,低剂量LPS具有激活巨噬细胞的潜力[25]。
本研究采用的成团泛菌(Pantoea agglomerans)来源LPS泛菌糖脂质在经口摄入或皮肤涂抹时炎症诱导潜力较低,且具有长期安全使用记录[19,20,37]。该菌常见于小麦、水稻等作物的根际,是被公认为促进植物生长的共生菌[38],可能通过自然饮食接触方式摄入,历经数代人[37]。
本研究通过体外实验初步证实:LPS激活的巨噬细胞可抑制人皮肤成纤维细胞的衰老并促进其年轻化。综上所述,LPS激活的巨噬细胞似乎具有双重作用:既能预防衰老,又可诱导衰老细胞的表型年轻化。据我们所知,这是首篇揭示巨噬细胞通过LPS刺激介导年轻化作用的研究报道。类似机制在糖尿病性痴呆的防治领域已有相关研究[29]。我们推测,巨噬细胞网络作为动态生物调控系统,介导LPS诱导的保护效应[19,20]。本研究中观察到的抗衰老与年轻化作用,可能是该网络功能的一个方面体现。
结论
本研究表明,经LPS激活的巨噬细胞能够抑制人皮肤成纤维细胞的衰老并促进其年轻化。这一发现颠覆了"LPS主要促进衰老和炎症"的传统观点。LPS激活巨噬细胞所展现出的抗衰老效应揭示了一种全新且出乎意料的机制,为开发针对细胞衰老的治疗策略开辟了新途径。未来研究应鉴定发挥上述效应的具体分泌因子,并利用皮肤衰老的体内模型对这些发现加以验证。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力