科学揭秘:肠道LPS如何通过“肝脑热线”,调控你的睡眠与体温!
本研究旨在探究LPS在大鼠体内的睡眠信号传导潜力
你是否曾经历过,在熬夜、压力大或饮食不规律后,不仅身体疲惫,睡眠也变得支离破碎,甚至伴有低烧般的不适?我们常常归咎于“免疫力下降”,但最新的科学研究揭示,这背后可能有一群意想不到的“信使”在操控——它们就来自你的肠道。
我们的肠道中居住着数以万亿计的微生物,它们不仅是消化的助手,更是一个巨大的化工厂,不断产生各类分子影响全身。科学家们发现,当一些细菌的“碎片”——比如革兰氏阴性菌细胞壁的主要成分脂多糖(LPS)——从肠道悄然“移位”进入肝脏门户(门静脉)区域时,它们会向大脑发送强烈的信号。
一项发表于权威期刊的研究,为我们解开了这个隐秘通讯的一角:只需极微量的LPS在门静脉内出现,就能显著延长睡眠时间,但同时也会引发发热。关键在于,这个效应高度局部化,全身给予同样物质则无效,这证明了肝脏区域存在着灵敏的“哨兵”。进一步研究发现,这一切是通过激活前列腺素系统来实现的,如同一个被触发的内部警报装置。
这意味着,高脂饮食、酒精、压力等日常挑战,都可能升高门静脉中LPS的水平,从而悄悄调整你的睡眠深度和体温节律。这不仅是细菌的“无心之举”,更可能是一套精密的肠道-肝脏-大脑对话机制的一部分。
今天,我们就来深入解读这项研究,看看肠道里的微生物如何通过LPS这把“钥匙”,远程影响你的睡眠与体温,重新理解那些日常生活中“说不清道不明”的不适感背后,微生物与人体复杂而深刻的共生关系。
LPS介导的微生物群对睡眠和体温的影响
摘要
背景
近期研究表明,从肠腔移位至宿主内环境的微生物分子可能在多种生理功能(包括睡眠)中发挥作用。我们先前研究发现,由肠道细菌产生的短链脂肪酸丁酸盐和革兰氏阳性菌细胞壁成分脂磷壁酸,在通过门静脉直接给药模拟其天然移位时,可诱导睡眠。基于这些发现,本研究我们旨在探究门静脉给予LPS(革兰氏阴性菌细胞壁的主要成分)在大鼠体内的睡眠信号传导潜力。
结果
低剂量LPS(1 µg /kg)可延长睡眠持续时间并加剧发热症状,但未引起全身性LPS水平变化。值得注意的是,在门静脉区域外以20倍剂量全身性给予LPS并不影响睡眠,这表明肝门静脉区域(包括门静脉和肝脏)对LPS的睡眠和发热效应具有局部敏感性。此外,前列腺素合成抑制剂吲哚美辛可抑制LPS的促眠和致热作用,而通过门静脉给予前列腺素E2或花生四烯酸可复制同样效应,表明前列腺素系统参与介导了这些作用。
结论
这些研究结果揭示了LPS在肝门静脉区域内对睡眠与发热机制的动态调控作用,进而促成了协调肠道菌群与大脑间通讯的复杂微生物分子体系。LPS是门静脉和门静脉外循环中血浆的生理成分,其水平会因高脂饮食、适量饮酒、睡眠不足和心理压力等日常挑战而升高。可能正是这些日常生活因素对人体产生的生理影响,从而凸显了微生物分子与宿主生理机能之间错综复杂的相互作用关系。
引言
越来越多的证据表明,肠道微生物群对宿主多种生理反应具有影响,这激发了人们对微生物分子在调控脑功能中所起作用的研究兴趣。微生物群与神经再生、行为、记忆及多种神经系统病理等基础脑过程密切相关(详见Ma等,2019年的综述)。例如,越来越多的研究揭示了,微生物群与阿尔茨海默病、帕金森病、抑郁症及焦虑症等疾病之间的关联。
大脑的睡眠机制与肠道菌群之间存在着动态双向关联。肠道菌群的减少会导致睡眠时间显著缩短,这证实了肠道菌群是诱发睡眠信号的重要来源(Brown等,1990;Millican等,2018;Ogawa等,2020)。反之,正常的睡眠-觉醒节律紊乱(如昼夜节律失调、急性睡眠缺失或慢性睡眠片段化)会影响菌群组成(Wang等,2021;Poroyko等,2016;Benedict等,2016;Voigt等,2016)。微生物分子长期以来因其通过全身或直接脑内给药诱导睡眠的能力而受到认可。其效应——如高剂量细菌细胞壁产物如肽聚糖片段(Krueger等,1982)、脂磷壁酸(LTA)(Szentirmai等,2021)和脂多糖(LPS)(Lancel等,1995;Kapas等,1998;Opp和Toth,1998;Szentirmai和Krueger,2014)所引起的效应,传统上背景下被解释为全身性炎症和疾病行为/综合征,因其与全身性细菌感染的体征和症状相似。
然而,学界观点正逐渐转变,开始将这些微生物成分视为宿主体内环境中固有的生理性要素,是血浆中正常存在的生理成分(Nolan, 1981; Wiedermann等, 1999; Goto等, 1994)。这些微生物代谢物通过肠腔向门静脉的移位进入循环系统,门静脉负责将富含营养物质和微生物分子的静脉血从肠道系统输送至肝脏(Guerville 和 Boudry ,2016)。脂多糖(LPS)作为革兰氏阴性细菌细胞壁的主要成分,由肠腔内分裂和死亡的细菌释放,并通过Toll样受体4(TLR4)介导的机制大量转移(Cetin 等,2004)。在健康状态下,LPS存在于门静脉及门静脉外体循环中,通过门静脉流入到达肝脏,肝脏作为LPS的“汇”,可以捕获并隔离循环中的LPS(Fox等, 1990)。
LPS及其他微生物分子从肠腔的易位受肠道屏障的调控(Guerville 和 Boudry,2016)。人们日常生活中遇到的诸多挑战会显著影响肠道屏障的完整性,进而改变循环中微生物分子的水平。例如,一顿高脂餐(Erridge 等,2007)、少量饮酒(Ferrier 等,2006;Sturm 等,2021)、睡眠不足(Wang 等,2021;Li 等,2024)或轻度心理应激(Vanuytsel 等,2013;Santos 等,2000)都会损害该屏障,使循环 LPS 水平升高。此外,菌群组成、细菌与肠黏膜的黏附、代谢产物生成以及循环LPS水平均存在昼夜波动,这进一步凸显了微生物群与宿主相互作用的动态特性(Cani 等,2007;Zarrinpar 等,2014;Thaiss 等,2016;Segers 等,2018)。
最新研究证实,易位的微生物分子可能对大脑功能(尤其是睡眠)发挥调节作用。例如,丁酸盐(一种由肠道细菌产生的短链脂肪酸)和LTA(一种革兰氏阳性细菌细胞壁成分)均可通过在肝门区域发挥作用来诱导睡眠(Szentirmai等,2021;Szentirmai等,2019)。在该区域发现的一种诱导睡眠的感觉机制,由此我们推测:源自肠道微生物群的易位LPS,可能通过相同或类似的机制参与睡眠调节。
我们的实验结果与上述假设一致:在不改变门静脉外循环血浆水平的剂量下,门静脉内注射LPS可有效诱导睡眠和发热。这种效应可被前列腺素合成抑制剂吲哚美辛所抑制,也可通过门静脉内给予前列腺素E2(PGE2)或前列腺素合成前体花生四烯酸来重现。这些发现有力表明,门静脉循环中的LPS动态影响着与睡眠和发热相关的机制,通过微生物分子组装促进肠道菌群与脑功能之间的通讯。
结果
实验1:门静脉注射LPS对睡眠、体温及运动活动的影响。
为评估门静脉注射LPS对睡眠及体温动态的影响,本研究测试了0.1-20 µg /kg的完整剂量范围(图1,表1)的作用效果。
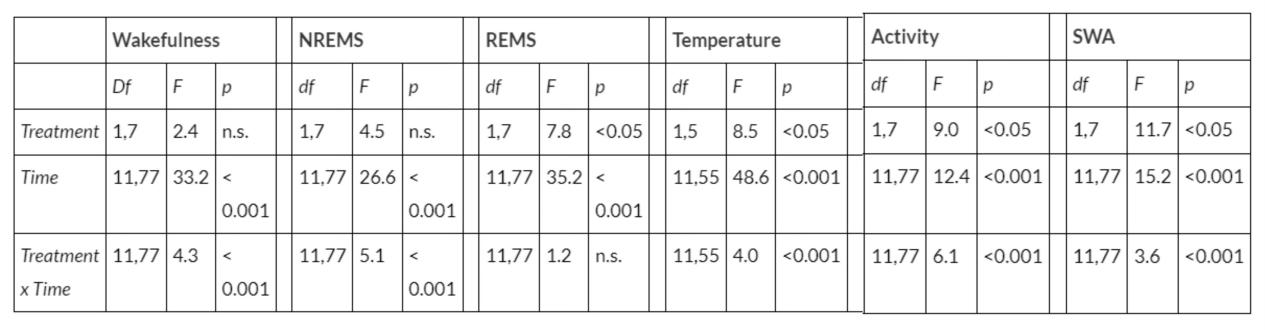
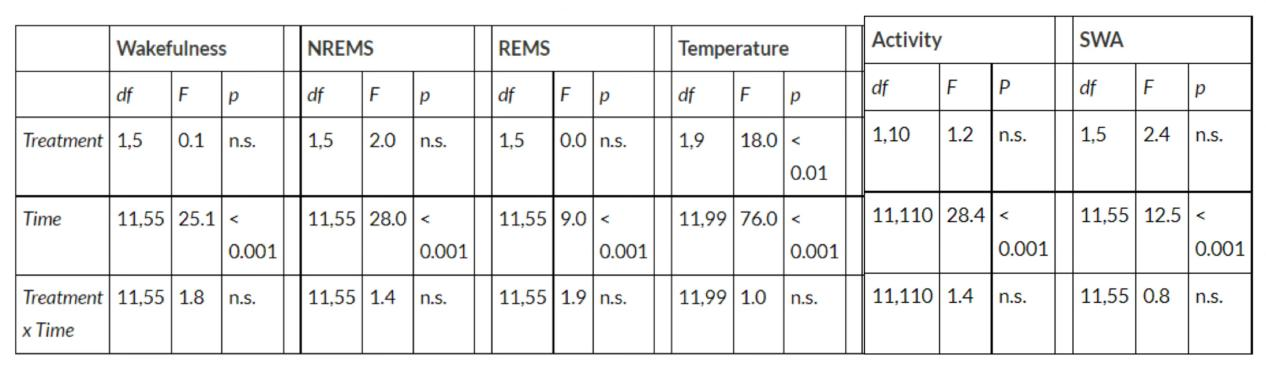
表1. 门静脉注射脂多糖(LPS)后,非快速眼动睡眠(NREMS)、快速眼动睡眠(REMS)、体温、运动活动及脑电图慢波活动(SWA)的统计结果:
0.1 mg/kg LPS,门静脉注射
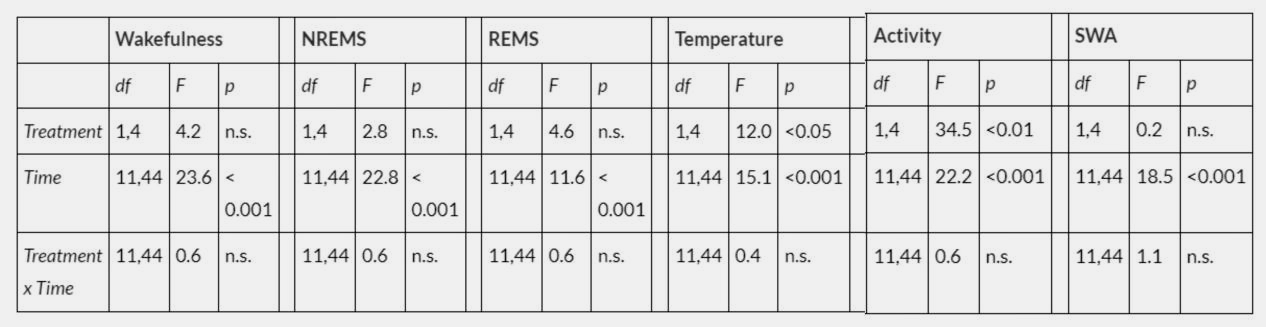
1 mg/kg LPS,门静脉注射
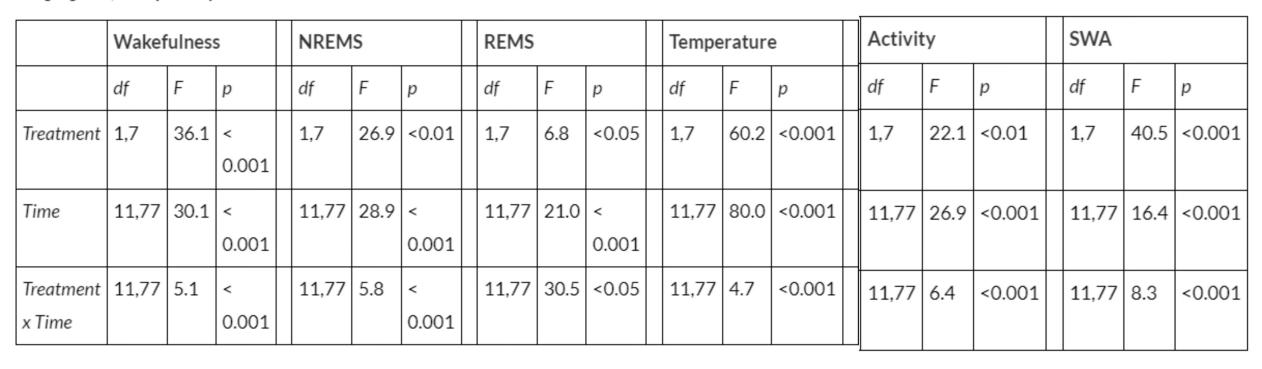
5mg/kg LPS,门静脉注射
20mg/kg LPS,门静脉注射
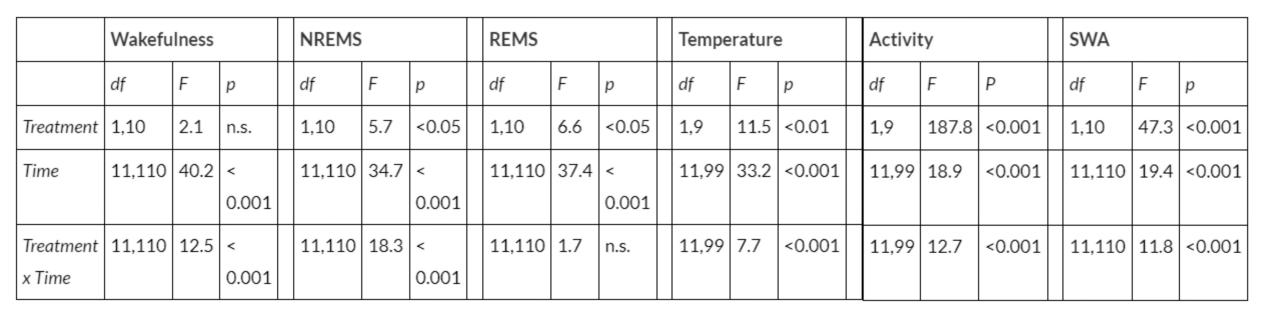
结果显示,经LPS处理后,非快速眼动睡眠(NREMS)时长显著增加,脑电图慢波活动(SWA)和运动活动则减少,这种变化在LPS处理后的最初12小时内尤为明显。这些效应在给药后约两小时开始显现。最低有效LPS剂量为1 µg /kg,可使黑暗期NREMS时长增加约40%(基线值:228.4 ± 11.6分钟 vs LPS组:315.1 ± 15.6分钟,p < 0.001,配对t检验)。更高剂量也观察到类似的NREMS效应。1 µg /kg LPS给药后,快速眼动睡眠(REMS)显著增加约70%(基线值:20.0 ± 3.0分钟 vs LPS组:33.6 ± 3.7分钟,p < 0.01,配对t检验)。20 µg /kg LPS给药后,黑暗期REMS减少,同时光照期出现NREMS的负向反弹。睡眠结构变得碎片化,具体表现为睡眠与觉醒次数增加、平均持续时长缩短(图2)。
图2.门静脉注射0.1、1、5和20 μg /kg脂多糖(LPS)、皮下注射20 μg /kgLPS、联合吲哚美辛预处理及门静脉注射1 μg /kgLPS对觉醒期、 NREMS 期和快速眼动睡眠期(REMS)发作次数及平均持续时间的影响。
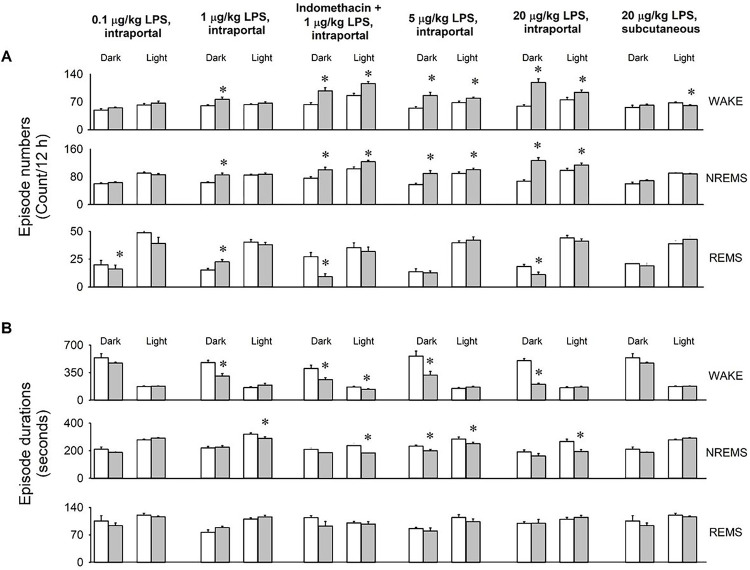
注射1和5 µg/kg LPS后,脑电图慢波活动(SWA)呈双相反应:最初两小时内出现短暂下降,随后恢复至基线水平,继而出现第二次持续时间较长的抑制。最高剂量引起的脑电图变化呈现类似动态,但在整个记录期间SWA始终未能恢复至基线水平。
值得注意的是,LPS在大约4小时的潜伏期后诱导了体温的持续升高。而在最高剂量下,升温之前先出现了一段低温期阶段。
实验2:门静脉注射LPS对门静脉外体循环LPS水平的影响。
门静脉注射1 µg/kg LPS并未引起颈静脉血LPS水平的显著变化。生理盐水注射后5分钟,血浆LPS浓度为0.47 ± 0.03 EU/ml;LPS注射后为0.45 ± 0.02 EU/ml(p = 0.64,配对t检验)。120分钟时,两组数值分别为0.65 ± 0.04和0.72 ± 0.04 EU/ml(p = 0.27,配对t检验)。与基线相比,120分钟样本显示LPS水平显著升高(Student‘s t检验,p < 0.01),这可能表明循环LPS水平存在昼夜波动变化。
实验3:LPS全身给药对睡眠、体温及运动活动的影响。
为验证肝门静脉区域对LPS具有高度敏感性,我们评估了门静脉外全身性给予LPS的作用效果,使用的剂量为经门静脉注射时可诱导睡眠的剂量(20 µg /kg LPS,皮下注射)。值得注意的是,该处理对睡眠-觉醒状态、脑电图慢波活动(SWA)或运动活动均未产生显著影响(图1)。方差分析显示,体温虽出现轻微但有统计学意义的处理效应(表2)。基线日平均体温为37.58°C,而LPS处理后体温小幅升高至37.69°C——24小时内升高了0.11°C。
图1.通过门静脉注射0.1、1、5及20 μg /kg脂多糖(LPS)、皮下注射20 μg /kg LPS,以及联合吲哚美辛预处理与门静脉注射1 μg /kg LPS,对大鼠觉醒状态、非快速眼动睡眠(NREMS)、快速眼动睡眠(REMS)、脑电图慢波活动(EEG SWA)、体温及运动活动的影响。
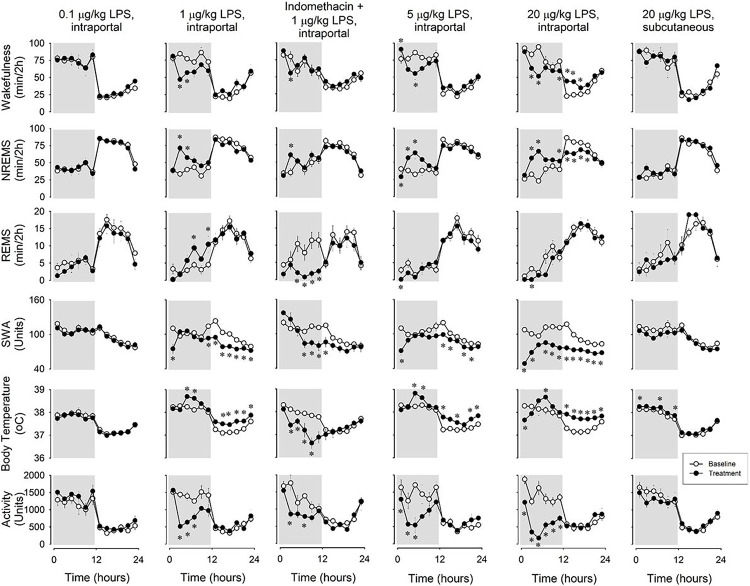
表2 .
皮下注射LPS对各项指标的影响:统计学结果(剂量:20 µg/kg,皮下注射)
指标包括:非快速眼动睡眠(NREMS)、快速眼动睡眠(REMS)、体温、运动活动及脑电图慢波活动(EEG SWA)。
实验4:吲哚美辛预处理对门静脉内LPS诱导的睡眠增加、体温升高及运动活动抑制的影响。
为评估前列腺素在门静脉给予LPS效应中的作用,我们在注射1 µg /kg LPS前,对实验动物进行了前列腺素合成抑制剂吲哚美辛的预处理。吲哚美辛显著抑制了LPS促进NREMS的作用,并完全阻断LPS诱导的体温升高和REMS增加(图1)。方差分析显示,预处理动物的 NREMS存在显著的“处理 × 时间”交互作用(见表3),尽管与未使用吲哚美辛预处理的LPS效应相比,这些效应显著减弱。在未使用吲哚美辛的情况下,LPS在12小时黑暗期内诱导NREMS量增加86.7 ± 15.6分钟。相比之下,经吲哚美辛预处理后,该增幅仅为38.0 ± 11.4分钟,表明LPS的效应存在显著差异(p < 0.05)。
吲哚美辛消除了1 µg/kg LPS给药后最初2小时内观察到的脑电图慢波活动(SWA)即时抑制,然而,在处理后第二个12小时期间出现的EEG SWA晚期抑制则未受影响。
未经预处理时,1 µg /kg LPS会导致快速眼动睡眠(REMS)和体温的升高。值得注意的是,吲哚美辛预处理使这两种反应均被逆转为显著抑制。LPS给药后12小时内REMS几乎完全消失,直到记录期的后半段才恢复至基线水平。体温在整个黑暗期持续下降,在LPS注射10小时后降至比基线低1.2°C的低体温状态。吲哚美辛预处理不影响LPS引起的运动活动反应降低。
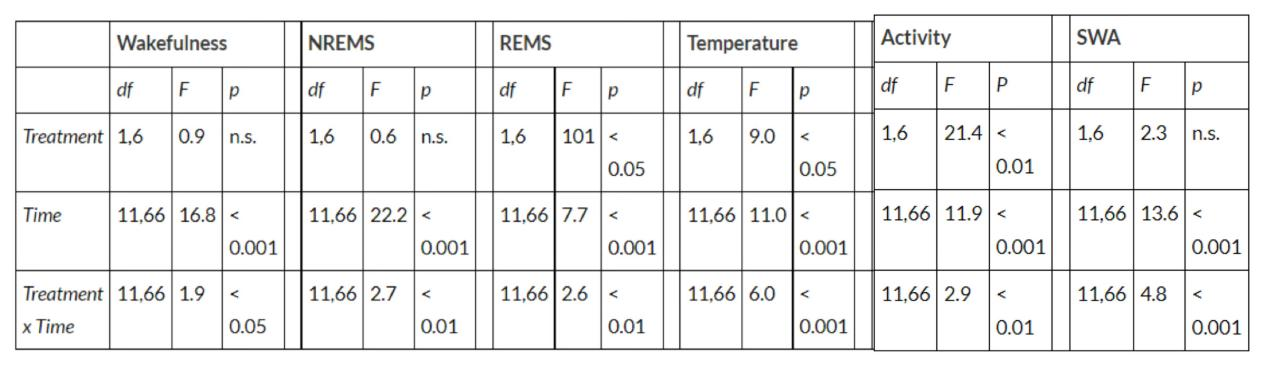
表3.
吲哚美辛预处理 + 门静脉注射1 µg/kg LPS的统计结果:
检测指标:非快速眼动睡眠(NREMS)、快速眼动睡眠(REMS)、体温、运动活动及脑电图慢波活动(EEG SWA)。
处理方式:吲哚美辛预处理后,经门静脉注射1 µg/kg LPS。
实验5:门静脉注射PGE₂与花生四烯酸(AA)对睡眠、体温和运动活动的影响。
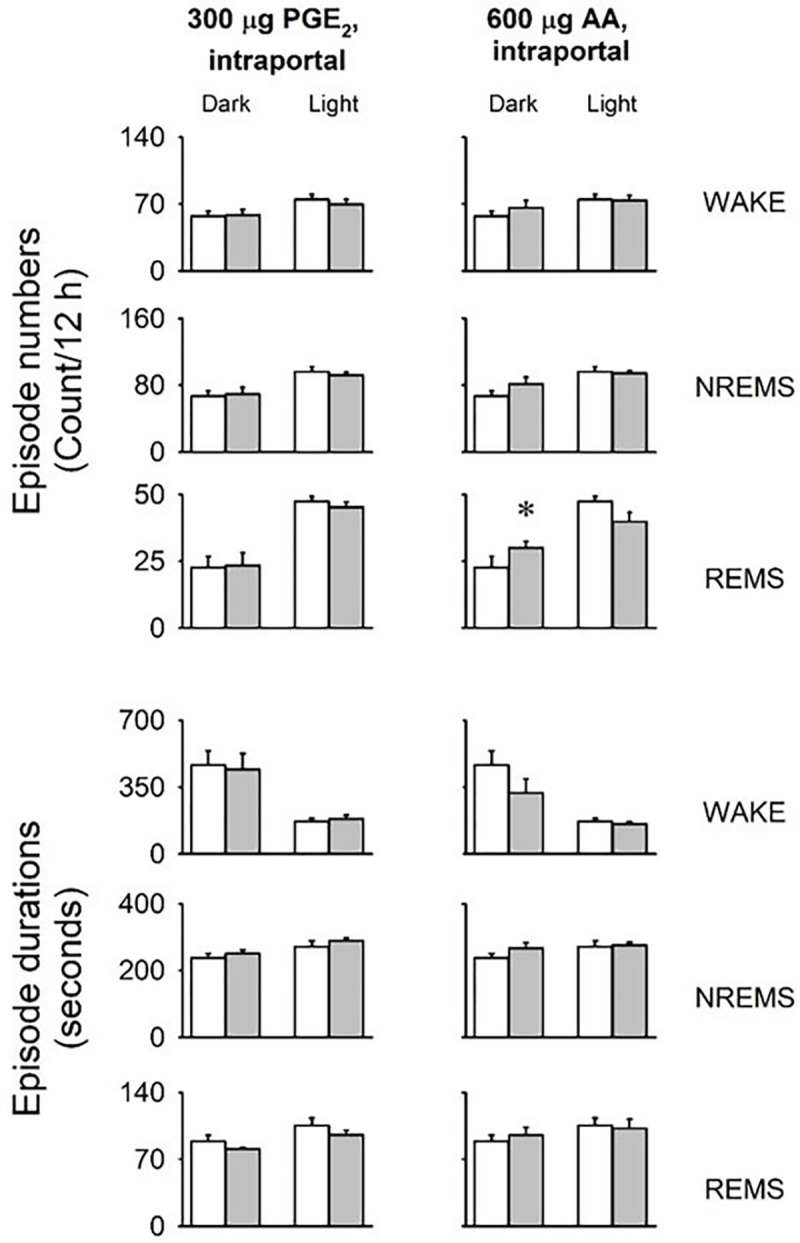
为验证门静脉给予PGE₂及其前体AA能否复现LPS诱导的效应,我们在注射后12小时内进行观察。结果两者均显著增加NREMS并降低体温(见图3、表4)。在暗期阶段,PGE₂使NREMS增加约22%,AA增加约36%(PGE₂基线值236.2 ± 31.0 min,处理后287.1 ± 29.5 min,p < 0.01;AA基线值264.6 ± 30.5 min,处理后358.6 ± 34.0 min,p < 0.05)。此外,AA处理后REMS有增加趋势(基线值34.7 ± 7.9 min,处理后47.1 ± 4.1 min,p = 0.057)。除AA给药后暗相期REMS发作次数增加外(图4),警觉状态次数及平均持续时间均未受干预影响。
PGE₂对脑电图慢波活动(EEG SWA)呈现出抑制作用,且在光照期观察到体温升高。虽然运动活动呈下降趋势,但PGE₂与AA给药均未引起统计学上的显著变化。
表4.
门静脉注射前列腺素E₂(PGE₂)与花生四烯酸(AA)后的统计结果:
检测指标:非快速眼动睡眠(NREMS)、快速眼动睡眠(REMS)、体温、运动活动及脑电图慢波活动(EEG SWA)。
处理方式:300 µg PGE₂,经门静脉给药。
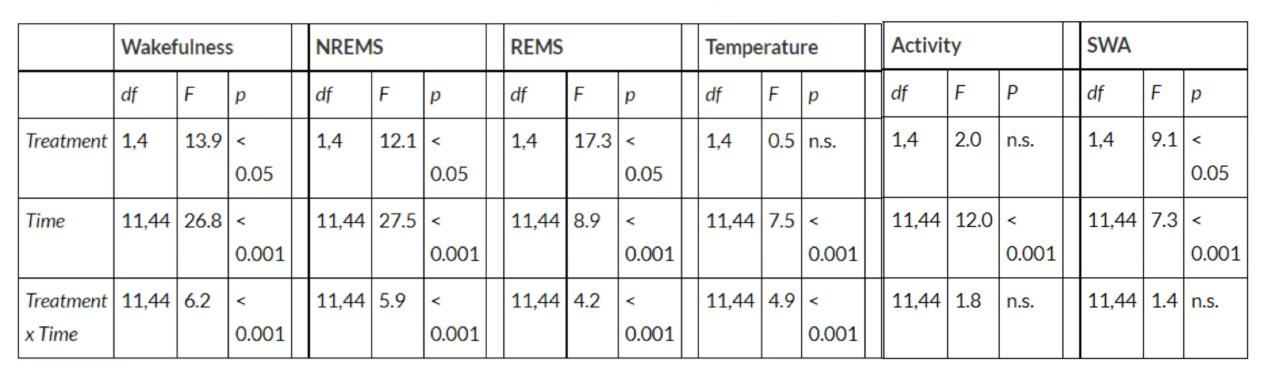
处理方式:600 µg AA,经门静脉给药。
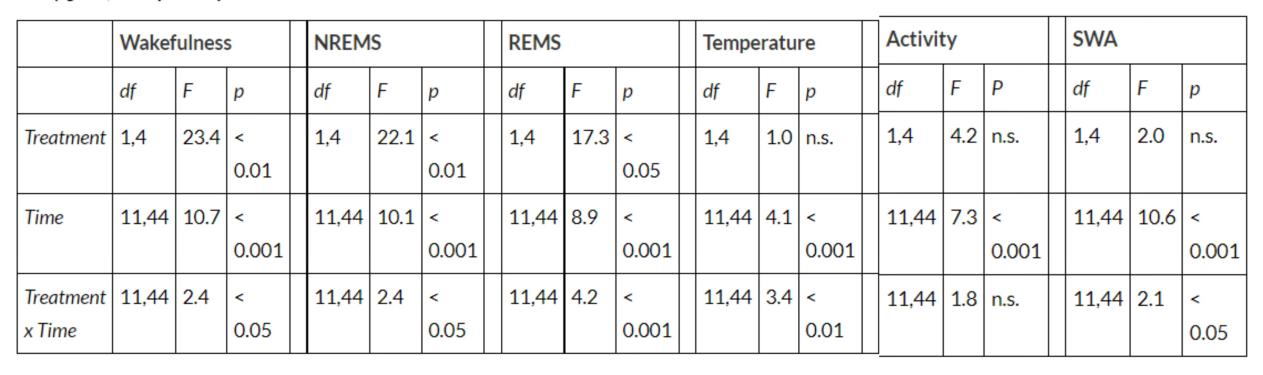
图3.
门静脉注射前列腺素E2(PGE2)和花生四烯酸(AA)对大鼠觉醒、 NREMS 、快速眼动睡眠(REMS)、脑电图慢波活动(SWA)、体温及运动活动的影响。
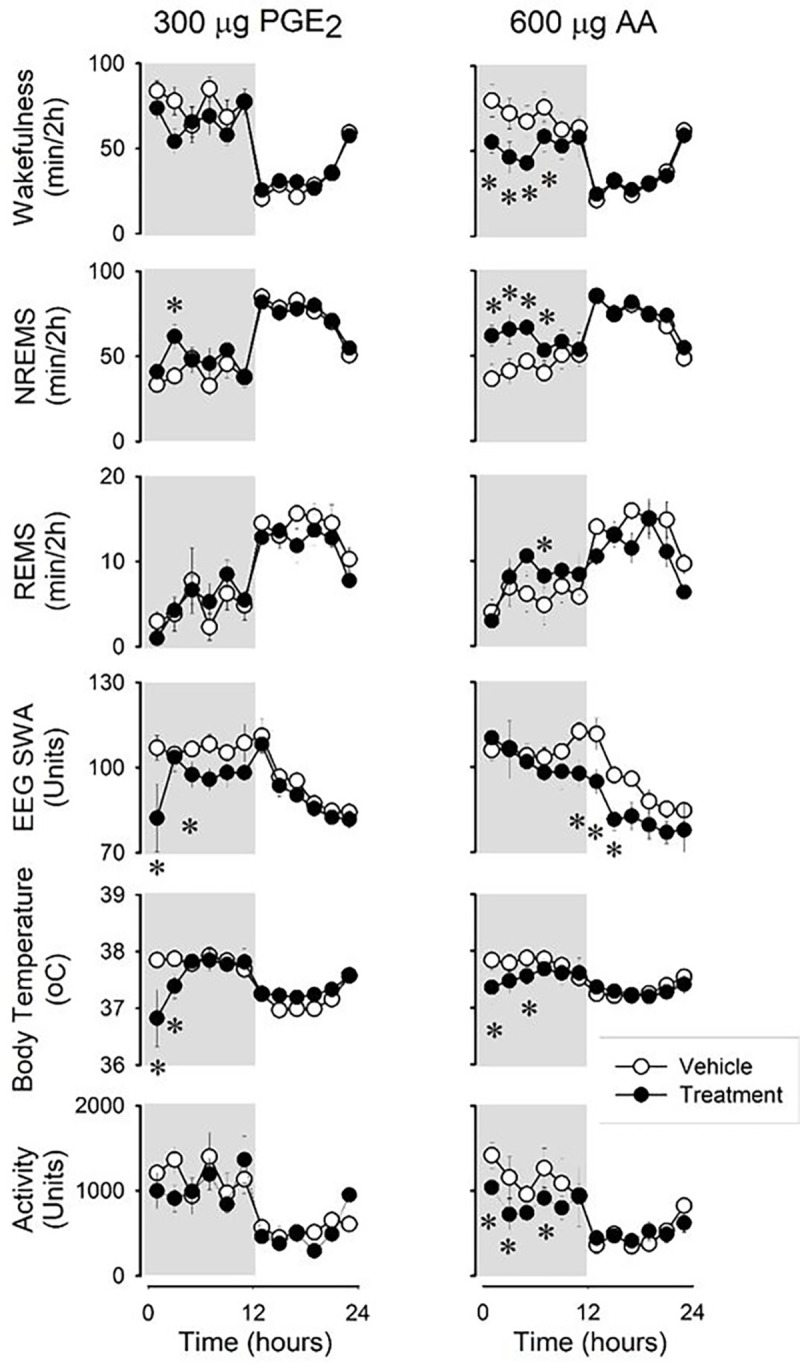
图4.
门静脉注射PGE2和花生四烯酸对觉醒次数、平均持续时间、 NREMS 及快速眼动睡眠(REMS)发作次数和平均持续时间的影响。
讨论
越来越多的证据支持“肠道菌群是促进睡眠信号的来源之一”这一观点(Brown 等,1990;Millican 等,2018;Ogawa 等,2020;Szentirmai 等,2019;Szentirmai 等,2021)。我们假设,革兰氏阴性菌细胞壁成分LPS可能作为此类促眠信号发挥作用。本研究主要发现显示:将LPS注入门静脉循环时,可诱导睡眠时间增加和体温升高。门静脉循环负责引流胃、小肠和大肠等肠道微生物群所在器官的血液。诸如LPS这样的微生物分子,通过一个称为“易位”的过程进入门静脉循环,从而进入宿主的内环境。肠道屏障虽可阻止微生物分子的游离移位,但在正常健康状态下,仍有大量此类分子出现在门静脉血液中(Guerville 和 Boudry ,2016)。LPS从肠腔向门静脉血液的易位,由与LPS受体TLR4相关的转运机制促进(Cetin 等,2004)。LPS天然存在于健康人类、大鼠和小鼠的门静脉及门静脉外的体循环血液中,使其成为原核生物来源的生理性血浆成分(Nolan ,1981; Wiedermann 等,1999; Goto 等,1994)。日常刺激会进一步促进转运,从而升高LPS的循环水平。例如,一餐摄入由三片涂有50 g黄油吐司的高脂餐,可使人体血浆LPS水平升高50%(Erridge 等,2007)。此外,常见情况如少量饮酒(Ferrier 等,2006; Sturm 等,2021)、急慢性睡眠不足(Wang 等,2021; Li 等,2024)以及轻度心理应激(Vanuytsel 等,2013; Santos 等,2000)都会导致循环LPS水平升高。
鉴于LPS在循环系统中普遍存在,且已有研究表明,全身性给予高剂量促炎性LPS可诱导包括人类在内的多种物种进入睡眠状态(Lancel 等,1995; Kapas 等,1998; Opp 和 Toth ,1998; Pollmacher 等,1993),我们提出假设:LPS向门静脉循环的转移可能作为肠道微生物群发出的信号来启动睡眠。若该假说成立,我们预期通过模拟增加LPS向门静脉循环的转移将促进睡眠。我们的研究结果支持了这一假设,表明即使仅向门静脉注射1 µg /kg的低剂量LPS,也能诱导非快速眼动睡眠(NREMS)增加和体温升高。
多项证据表明,门静脉注射LPS所产生的作用并非全身性,而是由位于门静脉循环或肝脏内的LPS受体激活所致。首先,我们既往研究已证实肝门静脉区域存在一种对微生物分子敏感的(如短链脂肪酸丁酸和革兰氏阳性菌细胞壁成分LTA)诱导睡眠的感觉机制(Szentirmai 等,2019; Szentirmai 等,2021)。其次,以最低有效门静脉剂量的20倍全身给予LPS,既未影响睡眠,也未引发体温产生任何生物学意义的变化。此外,在门静脉给药后,即使全身性给予最低有效剂量的LPS,也未能引起门静脉外体循环中LPS水平的变化。这一观察结果与肝脏作为高效LPS清除库的功能定位概念相一致。值得注意的是,1 g肝组织在单次通过中,可以1.5 µg/h的速率清除门静脉给予的LPS(Yamaguchi等,1982)。考虑到体重400g大鼠的肝脏重量约为14g(Webster 等,1947),其肝脏每小时可清除21µg LPS,即每分钟可清除0.35 µg 。在本实验中,我们在两分钟内注射了1 µg/kg LPS(相当于每只动物约0.4 µg LPS)。这些理论数据考量有力地支持了以下观点:低剂量LPS直接注入门静脉后,会被肝脏大量清除,不会导致溢出流入肝静脉。
在肝门区,存在多个潜在的LPS细胞靶点。LPS受体TLR4在多种肝脏细胞中均有表达,包括肝巨噬细胞(库普弗细胞)、肝窦内皮细胞、星状细胞和肝细胞(Nakamoto 和 Kanai,2014)。此外,肝脏与门静脉壁接受迷走神经传入神经支配,这些神经也表达TLR4受体(Berthoud 等,1992; Hosoi 等,2005; Kunda 等,2014)。鉴于LPS诱导的促睡眠和发热反应需经过2-4小时潜伏期才显现,这些效应不太可能是由LPS直接激活感觉神经所致。相反,这表明其作用机制涉及通过激活肝脏中较慢的生化机制来促进其他分子介质的产生。在各类肝细胞中,库普弗细胞是LPS作用研究中最为深入的靶点。库普弗细胞在响应LPS时,会产生已知可影响睡眠的分子,包括促炎细胞因子如白介素-6(IL-6)、肿瘤坏死因子-α(TNFα)以及前列腺素E₂(PGE₂)(Nakamoto 和 Kanai,2014;Bowers 等,1985;Peters 等,1990)。
我们未发表的初步数据显示,在环氧合酶-2(COX-2)基因敲除小鼠中,全身性给予LPS的促睡眠效应被完全消除,这促使我们进一步探究前列腺素在门静脉LPS介导效应中的作用。值得注意的是,使用COX抑制剂吲哚美辛预处理可显著抑制LPS的促眠作用,这凸显了前列腺素在介导这些效应中的关键作用。门静脉注射前列腺素E₂(PGE₂)及其前体花生四烯酸(AA)同样也表现出促睡眠效应,这一发现间接支持了肝脏前列腺素合成参与LPS诱导睡眠的过程。已有研究证实,外周产生的前列腺素具有促睡眠特性;烟酸作为皮肤角质形成细胞和朗格汉斯细胞中前列腺素合成的强效刺激剂,表现出显著的促睡眠效应。研究表明,烟酸诱导的睡眠可被吲哚美辛阻断(Szentirmai 和 Kapas ,2019)。
既往研究曾用小鼠研究探讨前列腺素在LPS促眠中的作用(Oishi 等,2015)。该研究发现,全身给予高剂量(约100 µg/kg)LPS的促眠效应不会被环氧合酶(COX)抑制剂美洛昔康阻断,且在神经系统缺乏EP3受体的小鼠、全身性微粒体前列腺素E合酶-1基因敲除小鼠或缺乏PGD₂受体DP型的小鼠中,该效应均未减弱。仅在神经系统特异性敲除EP4受体的小鼠中观察到促眠效应略有降低。然而必须强调,我们的模型与上述小鼠模型存在本质差异:本研究将低剂量LPS直接注入门静脉,未引起全身LPS水平变化;而上述研究采用全身高剂量给药,LPS可能抵达中枢及其他外周靶点。尽管LPS无法穿过血脑屏障(Banks和Robinson,2010),但它仍可作用于中枢部位(如脑血管内皮细胞)或血脑屏障不完整、对LPS通透的脑区神经元与胶质细胞(Matsumura等,1998;Blatteis等,1983)。当LPS到达这些中枢靶点时,可诱导发热和睡眠(Krueger 等,1986;Zielinski 等,2017;Steiner 和 Branco,2000)。此外,全身性给予高剂量LPS的促眠效应,还归因于棕色脂肪组织解偶联蛋白-1依赖的产热机制(Szentirmai 和 Kapas,2018)。LPS的这些中枢及肝外外周促眠效应,可能独立于前列腺素系统发挥作用。
低剂量LPS后观察到的快速眼动睡眠(REMS)增加,以及最高门静脉剂量后的REM睡眠抑制,与“全身给予递增剂量LPS会触发REMS抑制”的观点一致(Szentirmai 和 Krueger,2014)。吲哚美辛预处理同时抑制了体温和REMS,结合高剂量LPS同样抑制体温和REMS,这些观察结果表明REMS减少与体温变化之间可能存在关联。这与“实际体温调节变化本身可能参与睡眠调控”的概念相一致(Gilbert 等,2004)。
已有研究提出,肝脏前列腺素的生成是全身给予LPS引发发热的关键因素(Roth 和 Blatteis,2014)。我们的实验结果与这一观点一致。实验数据不仅显示睡眠时间延长,还揭示了经门静脉注射最低剂量LPS后体温也随之升高,这有力证明了LPS致热效应的作用位点位于肝脏。观察到的体温升高有4小时的延迟现象,可能归因于发热介质的“从头合成”。吲哚美辛完全消除发热反应,进一步凸显了前列腺素在此反应过程中的关键作用。
此外,吲哚美辛预处理不仅完全阻止了LPS诱导的发热,更有趣的是,它将这种反应转化为显著的低体温状态。在其他前列腺素生成被抑制的模型或IL-6、IL-10及NF-κB缺陷的小鼠中,也曾报道过类似的LPS低体温反应(Kozak等,1994;Zhang等,2003;Toth和Opp,2001;Morrow和Opp,2005;Jhaveri等,2006)。这些综合研究结果共同支持LPS对体温具有两种独立作用的观点(Dogan等,2002):它一方面通过激活促炎性IL-6/IL-10-PGE2-NF-κB轴促进发热,另一方面它又能独立诱导低体温。促炎通路的激活可能掩盖了低体温效应,而抑制促炎过程则会使低体温显现出来。此外,全身性给予更高剂量的LPS对体温呈现出双相效应,即在发热之前会出现一个初始的低体温阶段。LPS对体温的这种双重作用机制可能解释了观察到的双相反应。除“经典”LPS受体TLR4外,LPS还能与迷走神经传入纤维上的瞬时受体电位A1(TRPA1)受体结合并激活它(Meseguer等,2014)。膈下迷走神经干横断可消除高剂量LPS的低体温效应(Kapas等,1998),而IL-1或2-甲基-2-噻唑啉激活迷走神经TRPA1受体则会诱导低体温(Matsuo等,2021;Silverman等,2023)。因此,LPS的低体温作用可能是通过激活迷走神经TRPA1受体介导的。
脑电慢波活动(EEG SWA)反映非快眼动睡眠期(NREMS)δ波的出现频率。该指标受睡眠压力影响(Borbely等,2016),也可在睡眠-觉醒状态不变的情况下,因多种因素而发生改变,如阿托品等药物(Bradley,1968)、代谢变化(Lewis等,1974)或体温调节机制活动(Berger等,1998;Gaenshirt等,1954)。低剂量门静脉内给予LPS后观察到的双相SWA反应,与腹腔注射100 µg/kg LPS所观察到的反应相似(Kapas等,1998)。目前尚不清楚LPS诱导的脑电图EEG SWA抑制是源于NREMS压力降低,还是代表其对皮层神经元活动的“非睡眠”直接作用的影响。无论是哪种情况,该效应很可能源自肝门静脉区域,这一点通过门静脉外全身性LPS处理未见此效应得到证实。吲哚美辛可消除脑电图SWA抑制的第一阶段,表明前列腺素参与其中。我们先前报道,膈下迷走神经切断术可消除全身性LPS处理对脑电图EEG SWA的影响(Kapas等,1998)。此外,迷走神经刺激对脑电活动具有显著影响(Grastyan等,1952;Bonvallet和Sigg,1958;Chase等,1967)。这些观察结果支持以下观点:LPS对脑电图的影响可能至少部分是通过肝脏前列腺素生成引发的迷走传入神经介导。
吲哚美辛预处理未能完全阻止LPS诱导的睡眠,这表明除前列腺素外,其他介质也可能参与LPS的促眠效应。库普弗细胞、星状细胞和肝窦内皮细胞在LPS刺激下可产生TNF-α与IL-6(Seki等,2001;Thirunavukkarasu等,2005)。这两种细胞因子均具有促进非快速眼动睡眠(NREMS)的作用,可能参与了LPS的效应(Kapas等,1992;Szentirmai与Kapas,2019;Hogan等,2003)。这些介质可能通过肝静脉释放,并经体循环到达远端靶位。另一种可能是它们通过局部作用于传入神经元,因为迷走神经和脊神经均向肝脏提供传入神经支配。迷走传入神经表达PGE₂受体EP3和EP4以及TNFα p55受体(Hermann等,2005;Steinberg等,2016;Ek等,1998)。PGE₂与TNF-α均能刺激迷走传入神经活动(Birrell等,2013;Hermann等,2005)。因此,局部生成的PGE₂及其他介质可能刺激迷走传入神经向大脑核心睡眠回路发送促眠信号。这一机制与以下发现一致:迷走神经向大脑传递诱导睡眠的输入信号(Armitage等,2003;Bonvallet与Sigg,1958),且全身给予高剂量LPS的促眠及致热作用可被迷走神经横断所抑制(Kapas等,1998;Opp与Toth,1998)。
综上所述,我们的研究结果有力支持了以下观点:从肠道腔易位至门静脉循环的LPS在调节睡眠和体温中发挥重要作用。我们提出,LPS与其他细菌代谢物(如丁酸盐和LTA)以及多种潜在微生物分子协同作用,共同构成了一套针对肝脏的复杂分子信号传导网络,从而激活肝门静脉传感器。这些传感器产生的信号可能通过神经或体液途径,传递至中枢睡眠回路。这种多层面的分子相互作用,凸显了肠道菌群、微生物分子与睡眠-觉醒周期调控之间精密而复杂的联系。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力