破解胃溃疡防护难题:从传统食养到科学护胃,LPS为“药食同源”翻开新页!
LPS对胃溃疡的保护作用与其他来源LPS的比较研究
在现代快节奏的生活中,胃部不适已成为许多人的“隐形伴侣”,而胃溃疡更是其中不容忽视的健康警报。科学家们将目光投向了人体自身的防御系统——尤其是被称为“免疫哨兵”的巨噬细胞,探索如何通过安全地激活它来维持机体稳态,从而对抗疾病。
今天分享的这项研究,正是这一探索中的前沿一章。它聚焦于一种从日常小麦粉中提取的特殊物质——小麦粉脂多糖(LPSw)。研究团队进行了一场精细的“对比实验”,将LPSw与多种细菌来源的脂多糖同台较量,通过严谨的小鼠模型,深入检验了它们通过不同途径(注射与口服)对抗胃溃疡的保护效力。
令人惊喜的是,这项发表于专业领域的研究发现,这种来源于食物的LPSw,在通过简单的口服方式(尤其是自由饮水摄入)时,展现出了不输于甚至更适宜日常应用的显著保护效果。这不仅为理解“药食同源”提供了现代科学的注脚,也为寻找更温和、更依从性的日常健康支持方案打开了新的思路。
让我们一起走进这项研究,看科学如何从平凡的食物中,发现不平凡的守护之力。
活化巨噬细胞调节的稳态。III. 小麦粉脂多糖(LPSw)对小鼠胃溃疡的保护作用与其他来源LPS的比较研究
本研究通过小鼠实验,采用肠外注射和口服两种途径,考察了不同来源脂多糖(LPS)对胃溃疡的保护作用。实验采用吲哚美辛、应激或酒精诱导小鼠胃溃疡模型。实验所用LPS分别制备自6种细菌(大肠杆菌、成团泛菌、无花果沙雷菌、阴沟肠杆菌、百日咳博德特菌、粪产碱杆菌)及小麦粉中提取。静脉注射实验显示,成团泛菌LPS在所有受试组中效果最佳。而小麦粉脂多糖(LPSw)通过口服途径(尤其是以自由摄取方式添加至饮用水中)表现出显著的保护作用。
关键词 胃溃疡;脂多糖;巨噬细胞活化;稳态;成团泛菌
引言
我们先前提出,胚胎发育过程中由肿瘤坏死因子(TNF)驱动的炎症——我们称之为“个体发生性炎症”(ontogenic inflammation)¹,只要在成年期适当重现,就能调节机体的稳态。在本系列先前的研究报告中²,我们描述了从小麦粉中提取的脂多糖(LPSw)也能再现这种个体发生炎症。目前已知的LPS种类繁多,其中大多数来源于革兰氏阴性菌。在本研究报告旨在阐明LPSw对小鼠胃溃疡的保护作用,并将其效果与其他多种LPS进行比较。通过吲哚美辛、应激或乙醇刺激在常规大鼠模型中诱发小鼠胃溃疡³。采用肠外和口服途径检测每种LPS的抗溃疡效果。结果显示,所有受试的LPS在静脉给药时均表现出一定程度的抗溃疡效果;而LPSw在通过饮水自由摄取的口服摄入时,展现出显著的抗溃疡保护效果。
结果
不同LPS经静脉途径对小鼠胃溃疡的保护作用
用IM检测抗溃疡指数(图1)。静脉注射时,每只小鼠的1 μg的 LPSw可显著预防降低溃疡的发生率(p<0.01)。其他LPS也显示出类似的效果(表I),效果依次为:LPSw、B. pert.的LPS、成团泛菌(P. aggl.)LPS、S. fic.的LPS,这些效果均优于大肠杆菌和阴沟肠杆菌LPS。
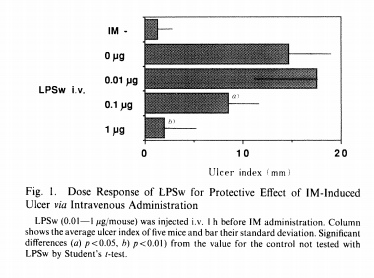
图1. LPSw通过静脉给药对IM诱导性溃疡保护作用的剂量反应
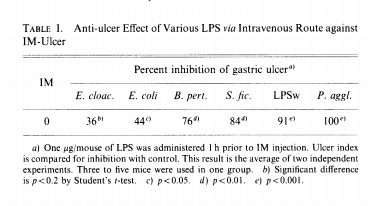
表1. 静脉注射不同来源LPS对IM诱导溃疡的抗溃疡作用
图2显示LPSw最佳给药时机:在IM处理前1小时静脉注射有效,IM处理后再给药则无效。拟用于口服途径的粗提LPSw样品(LPSw-H)静脉注射同样有效(表II)。
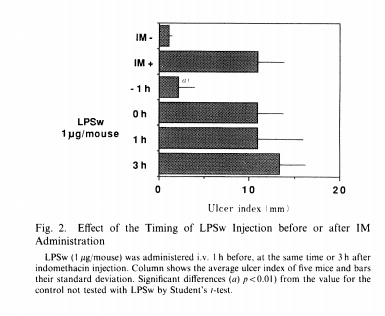
图2. LPSw在IM给药前后不同注射时机对其效果的影响
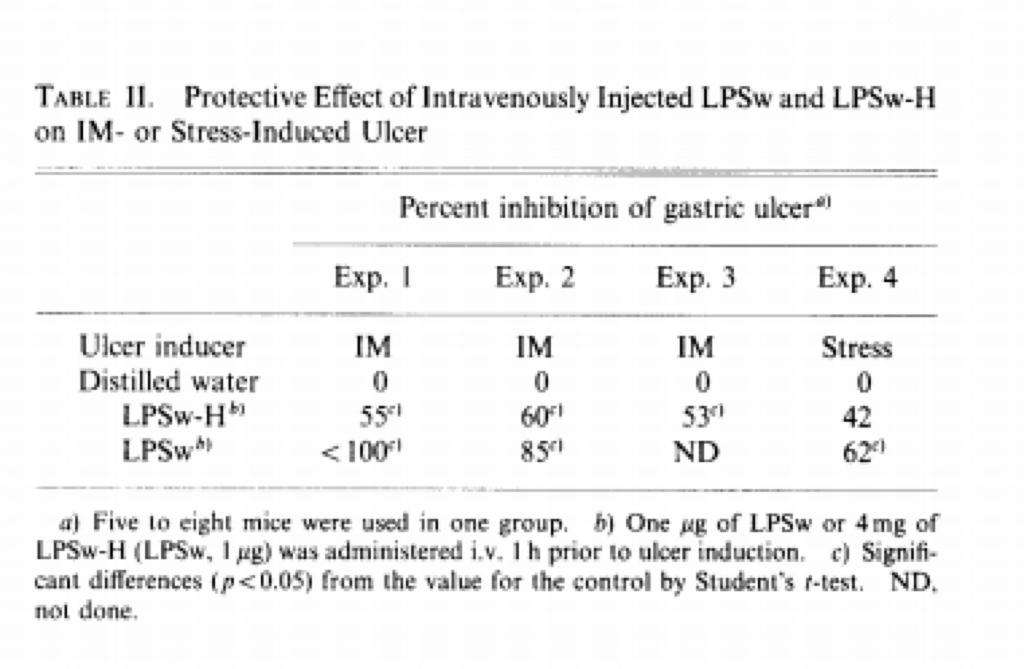
表2. 静脉注射LPSw与LPSw-H对IM诱导或应激诱导溃疡的保护作用
不同LPS经口服途径对小鼠胃溃疡的保护作用
鉴于溃疡部位的特殊性,口服途径可能更有利于对胃溃疡的防护。本研究比较了LPSw与4种不同来源的LPS口服效果。LPSw采用其粗提物LPSw-H进行测试。表III汇总了6项独立实验中LPSw-H的抑制率(以溃疡发生率百分比表示)。实验采用的胃溃疡模型包括IM型、水应激型和乙醇诱导型,在6种实验情况下均观察到约50%的抑制效果。作为对照的H2受体阻断剂西咪替丁⁷也显示出类似效果。图3展示了为确定LPSw-H最佳给药时机的测试结果:在IM处理前1小时口服最为有效。表IV列出了5种LPS(包括B.pert.、P.aggl.、A. faec.、LPSw、E.coli)经口服途径的抗溃疡活性。SDS-PAGE检测的LPS分子大小与抑制效果呈正相关。
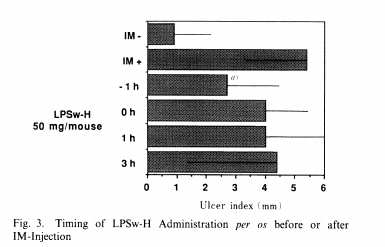
图3. LPSw-H口服给药(IM注射前或后)的时间安排
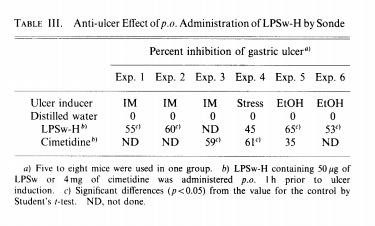
表3. LPSw-H经口服给药的抗溃疡作用

表4. 各种LPSs的口服抗溃疡作用及其SDS-PAGE图谱分析
各种LPS的半数致死量(LD₅₀)与抗溃疡活性比较
测定了4种LPS的LD₅₀。表V汇总了LD₅₀数据,并与各自的抗溃疡活性进行对比。LPSw的LD₅₀与大肠杆菌LPS及成团泛菌LPS相当。在口服给药的情况下,由于小麦粉本身无害,LPSw-H可能是最理想的材料。

表5. 4种来源的纯化LPS的LD₅₀
LPSw-H自由摄取对小鼠胃溃疡的保护作用
在小鼠自由摄取LPSw-H的条件下,测试其对胃溃疡的保护效果。图4显示了结果,表明LPSw-H可显著降低由IM诱发及应激诱导的溃疡发生率,具有显著的保护作用。
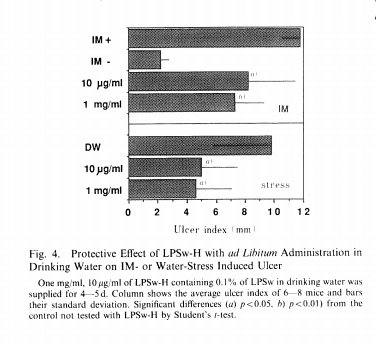
图4. 通过饮水自由摄取LPSw-H对IM或水应激诱导溃疡的保护作用
讨论
小麦粉来源的新型脂多糖LPSw²,无论溃疡诱导剂是IM、水应激还是乙醇,已证明即使口服,也能对溃疡的发生起到保护作用(表II、III)。
LPSw-H显著的抗溃疡活性与西咪替丁⁷相当(表III),而后者是目前最有效的市售抗溃疡药物之一⁷。这些事实表明,LPSw-H具备适用于临床溃疡治疗的潜力。
如表I所示,静脉注射最有效的抗溃疡LPS来自成团泛菌(Pantoea agglomerans)的LPS——已知该菌是小麦、棉花等植物中常见的伴生革兰氏阴性菌⁸。我们发现,成团泛菌LPS在诱导内源性TNF产生的“启动状态”方面也最为有效(数据未显示)。因此,成团泛菌LPS可能是肠外给药中最有应用前景的LPS。
如表IV所示,口服途径最有效的LPS是B.pert. LPS。另一方面,LPSw-H作为小麦粉提取物,可每日摄取且无害,因而在长期预防溃疡方面比B.pert.LPS更安全、更实用。
本研究比较了来源于不同种类革兰氏阴性菌来源LPSs对应激、IM、水应激及乙醇诱导的胃溃疡发生的保护作用。我们改进原有的大鼠实验系统³,新建立了一种检测方法。可同时比较6种不同LPS的保护效果(表I)。
LPSw 的确切作用机制尚不明确。然而,被激活至内源性TNF生成“启动状态”的巨噬细胞可能是效应细胞。一般而言,如本研究所示,即使在低剂量(1μg/小鼠)下,LPS也能将巨噬细胞激活至此阶段²。我们还曾证明,启动至内源性TNF生成的巨噬细胞会产生26 kDa的前体TNF,这些前体可能附着在活化巨噬细胞表面⁹。巨噬细胞激活后生成的前列腺素E₂,也可能是阻止胃溃疡发生的效应分子之一¹⁰。
本研究表明,有两种LPS值得被筛选出来,用于进一步验证其对疑难疾病的治疗效果。一种是口服用的LPSw,另一种是经皮或通过其他肠外方式使用的成团泛菌(Pantoea agglomerans)LPS。
免责声明
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力