途径决定效应:解读LPS“静脉成劫,口服为何是解”?
口服LPS预防多种疾病:益处与应用价值
口服LPS的有益作用与应用价值
引言:
在医学常识里,脂多糖(LPS)常常与“炎症”、“中毒”紧密相连。静脉注射极少剂量,就可能在人体内引发剧烈反应。然而,自然与我们开的这个“玩笑”背后,却隐藏着健康的深层智慧:当LPS通过我们与生俱来的“口服-肠道”黏膜途径进入体内时,故事完全不同了。
研究表明,口服高剂量LPS对动物安全无毒,不仅不会引起全身炎症,反而对过敏、代谢等多种现代疾病展现出显著的预防与改善潜力。这揭示了一个关键事实:摄入途径,决定了LPS是“毒药”还是“良方”。
其实,LPS离我们并不遥远。它广泛存在于日常食物和人体肠道庞大的菌群中,是我们一生持续接触的“老朋友”。这种温和的、持续的接触,很可能正是训练与平衡我们免疫系统、构筑健康防线的重要方式。
那么,口服LPS究竟如何在体内行使其“健康卫士”的职能?科学家发现,它并非通过引发炎症来工作,而是巧妙地启动一个名为“预激”的免疫准备阶段,并可能通过细胞间直接对话的 “巨噬细胞网络” ,温和地调节全身平衡。
口服 LPS 到底是伪概念还是新风口?本文将带你走进这个颠覆认知的研究领域,解析口服LPS如何从一种潜在的“毒素”,转变为预防多种疾病的希望之星,并展望它守护我们未来健康的广阔前景。
口服LPS预防多种疾病:益处与应用价值
摘要
众所周知,静脉注射脂多糖(LPS)会在哺乳动物中引起严重的毒性反应。据报道,人体静脉注射LPS的最大耐受剂量仅为1–4 ng/kg 体重。然而,口服高剂量的LPS在其他哺乳动物、鸟类或鱼类中未引起毒性或全身性炎症。在大鼠实验中,连续两周口服高剂量LPS(2 mg/kg)没有引起毒性。此外,多项实验表明,口服LPS对多种疾病(包括过敏性疾病及生活方式相关疾病等)具有预防和改善作用。这些结果表明,黏膜途径给予LPS在生物反应中通过不同于肠外给药的调控机制发挥作用。尽管口服LPS在疾病预防领域前景广阔,但目前应用仍不广泛。为拓展口服LPS在预防生活方式相关疾病和过敏性疾病中的应用,有必要阐明口服LPS激活免疫反应的具体机制。本文简要综述近期关于口服LPS应用价值的研究进展。
LPS的结构
脂多糖(LPS)是革兰氏阴性细菌外膜的主要成分,由于其含有亲水性多糖和疏水性脂质部分而具有两亲性。其基本结构由三部分组成:(I)脂质A,(ii)核心糖,(iii)和O抗原(O-多糖)。脂质A由4至7个脂肪酸链结合两个葡糖胺组成,并通过高度保守的8碳糖——酮脱氧辛酸(KDO)与核心多糖连接。核心区域是一种含有特征性糖残基(KDO 和庚糖)的寡糖,其化学变异较O抗原更为有限。脂质A作为膜锚定物发挥作用(图1)。
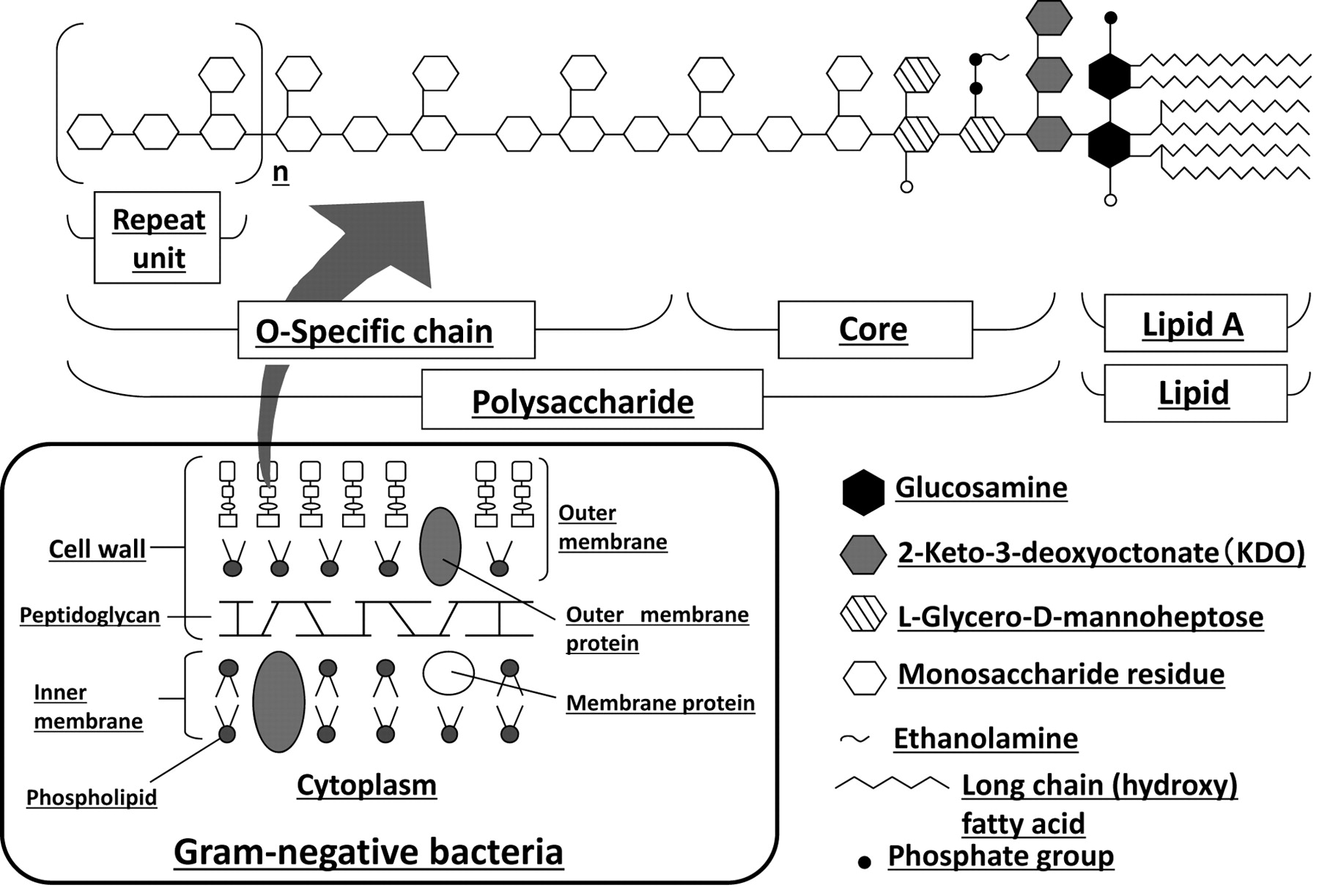
图一.LPS的基本结构。
LPS之所以触发免疫应答,是因为它能与免疫细胞及部分上皮细胞的受体结合,并通过胞内信号激活核转录因子。学界普遍认为,在LPS结合蛋白(LBP)催化转移LPS单体后,CD14可作为LPS的高亲和力受体,形成CD14–LPS复合物(1)。Toll样受体(TLRs)的结构与功能在先天免疫中至关重要。免疫细胞能够识别病原体上的特定结构,例如肽聚糖、脂多糖、β-1,3葡聚糖、双链RNA以及非甲基化的CpG DNA(1, 2)。
CD14、TLR-4和骨髓分化因子-2 (MD2)的复合物具有极高的敏感性,能够通过0.1 ng/ml浓度的LPS–LBP复合物(3)即可诱导细胞内信号传导。因此,促炎细胞因子如肿瘤坏死因子(TNF)- α 、白细胞介素(IL)- 1β 和IL-6被树突状细胞(DCs)、T细胞和B细胞、粒细胞、自然杀伤细胞以及巨噬细胞诱导并激活为免疫应答。
学界普遍认为,LPS的脂质A组分是介导其生物活性的关键结构。然而,我们近期利用针对LPS中O-多糖组分的特异性单克隆抗体进行的研究表明,O-多糖链对LPS功能同样具有重要作用。该功能可能通过一种与LPS受体结合的凝集素样衔接分子实现,其作用机制或与已知的β-1,3葡聚糖结合分子(如与TLR-2关联的dectins家族受体)相似(4)。但迄今为止,尚未有研究能明确识别LPS中O-多糖组分的特异性受体。
静脉注射LPS的生物活性
Otto等人报告了一项关于静脉注射LPS发挥抗肿瘤作用的临床试验,该研究试验纳入了27例晚期结直肠癌患者(5)。在这些患者中,观察到1例完全缓解和2例部分缓解;但静脉注射LPS引发了短暂的肾毒性和肝毒性反应。一项Ⅰ期研究将马流产沙门氏菌LPS在人体静脉给药的最大耐受剂量确定为 1–4 ng/kg(6,7)。严重的全身性副作用,如发热(世界卫生组织Ⅲ级)、寒战和低血压,是剂量限制性毒性(6,8)。小鼠静脉注射LPS的急性毒性剂量为4–8 mg/kg,半数致死量(LD₅₀)亦在此范围内(9)。上述结果表明,LPS静脉给药通过引发全身性炎症导致严重毒性,但通过激活先天免疫系统预期会产生一些有益的抗肿瘤作用。
体外观察到的免疫细胞对LPS高度敏感的细胞反应,同样说明静脉注射LPS可在体内诱发免疫应答。当静脉注射LPS时,会引发血清C反应蛋白、 TNF - α 、IL- 1β 和IL-6呈剂量依赖性升高,进而引发高热、腹泻、呕吐和低血压(10)。若预先用二氯亚甲基二膦酸盐脂质体(Cl₂MDP-liposomes)进行预处理,再静脉注射LPS,则可显著降低死亡率(从55%降至14%)(11)。因此,LPS致死性毒性的发病机制,源于激活的巨噬细胞系统性过度释放促炎细胞因子所引发的全身性炎症反应。
关于LPS的体内去向:静脉注射后数分钟即可在血浆中检测到LPS,其中大部分被转运至肝脏进行代谢降解;少量血浆LPS在脾脏、肺脏、肾脏及肾上腺中代谢,并最终通过粪便排出体外(12)。
口服LPS的生物效应
与肠外给药相比,口服LPS显示出完全不同的结果。Oketani等人指出,口服LPS对动物无害(13)。Schryvers等人发现,小鼠连续40天摄入20 μg/ml的LPS未出现毒性证据(14)。Illyés等人报告称,重复口服高剂量大肠杆菌LPS对大鼠小肠结构和细胞增殖无明显影响(15)。我们的研究也证实,单次口服高剂量成团泛菌LPS(600 mg/kg)对大鼠无副作用(16)。此外,连续28天口服300 mg/kg该LPS(约为动物(人、鸡和鱼)推荐LPS摄入量10 μg/kg的30,000倍),在大鼠中仍未出现肝毒性、肾毒性、炎症或体重下降的证据。这些发现表明,口服LPS对动物是非常安全的。
已有研究报道了口服LPS引发的生物反应。Murakami等人发现,在正常C57BL/6小鼠中,口服沙门氏菌LPS(100 μg/只)7天后,肠道固有层和腹腔内的 B-1 细胞被激活(17)。由于B-1细胞在体外和体内均能摄取凋亡的胸腺细胞和大肠杆菌(18),它们被认为是一种吞噬细胞,且具有与吞噬细胞相似的分化潜能(19)。Chen等人报道,口服大肠杆菌LPS(饮用水含10 μg/ml)可保护严重烧伤小鼠,防止因使用抗菌药物而导致的细菌移位和腹腔巨噬细胞功能抑制(20)。表明口服LPS具有保护机体免受肠道细菌感染的有益特性。Masuda等人指出,LPS 可诱导 Paneth 细胞分泌 cryptdin-4(21),该物质是防御素中杀菌活性最强的一种(22)。Rakoff-Nahoum等人证实,口服LPS可挽救共生菌耗竭小鼠免于DSS诱导的死亡(23)。Márquez-Velasco 等人亦发现,对接受盲肠结扎穿孔术的小鼠进行预防性口服LPS,可显著提高其存活率并减轻靶器官的炎症反应(24)。
我们已有研究报道,小麦粉的热水提取物(经口服)含有源自革兰氏阴性植物共生细菌(如成团泛菌)的巨噬细胞激活物质。该菌的LPS被命名为IP-PA1,是主要的巨噬细胞激活物质(25,26)。研究表明,该物质在人类和动物模型中均能有效预防生活方式相关疾病、过敏性疾病及感染性疾病。口服成团泛菌LPS有助于预防高脂血症(兔模型)(27)、糖尿病(小鼠和人类)(28)、多种感染性疾病(小鼠和虾模型)(25,29,30)以及溃疡性结肠炎(小鼠模型)(31),并能(小鼠、大鼠和人类模型)产生镇痛效果(32-34)。
LPS经肠道途径口服给药的可能途径
Benoit等人曾报道,纯化的LPS在体外实验中无法透过肠黏膜(35)。然而,其他研究显示,动物口服LPS后体内可检测到LPS含量显著增加(36-38)。据估算,使用¹²⁵I标记的LPS进行实验时,口服剂量的0.1%至0.25%可在血液中被检出。若按此吸收比例计算,口服1 mg LPS后,理论上应有1至2 μg 的LPS存在于血液中(36)。该剂量通过静脉注射在小鼠体内足以引发显著的全身性炎症反应,但口服1 mg的 LPS并未观察到游离细胞因子水平的升高(未发表数据)。基于这些结果,我们确定口服LPS在肠道的吸收机制与静脉给药存在差异。近期研究报道的小肠黏膜途径摄取LPS的可能机制总结于图2(20,36,39-44)。
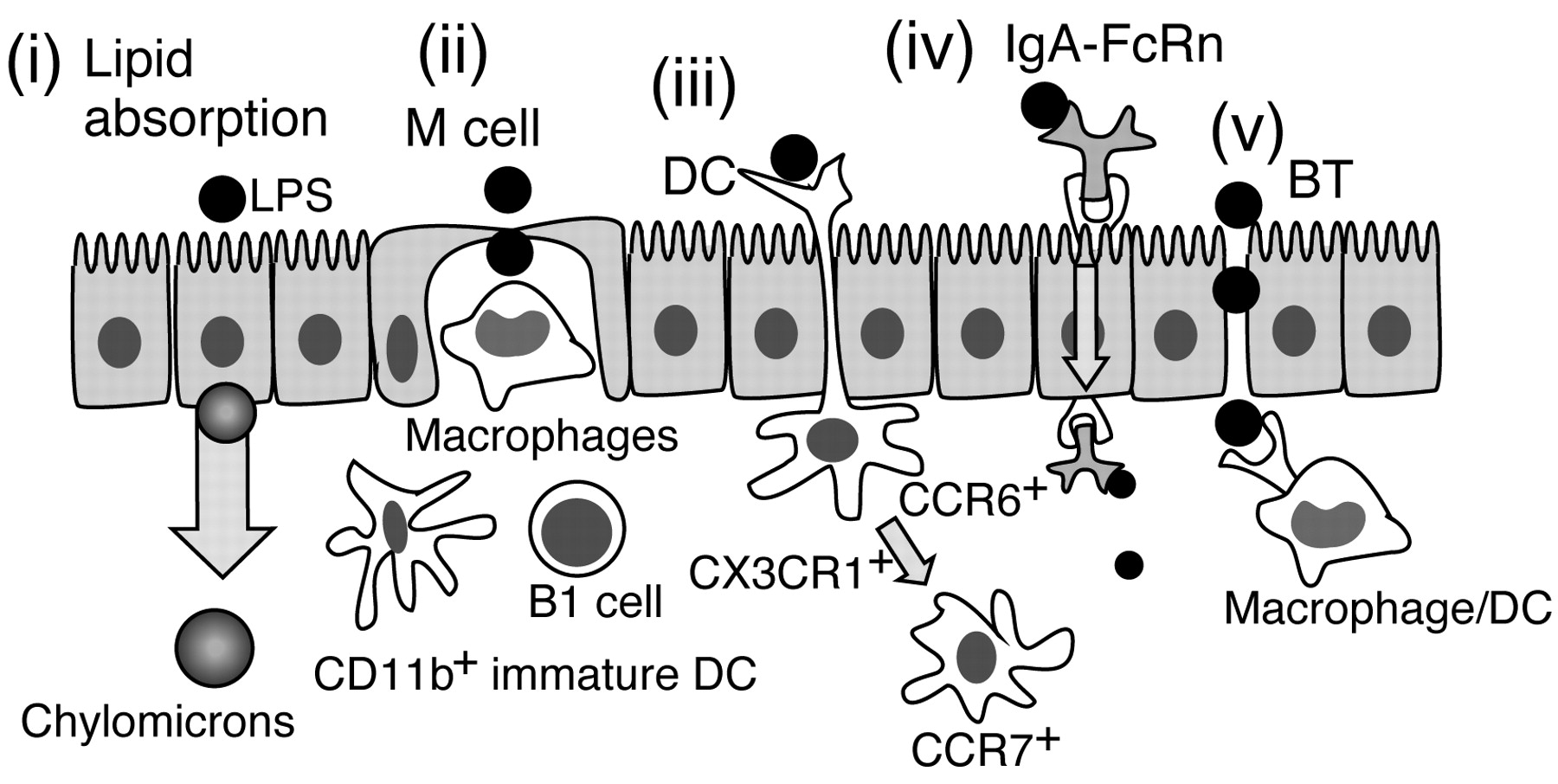
图二. 肠黏膜摄入LPS的可能途径
这些LPS易位途径可能使其渗透到淋巴组织中,如派尔集合淋巴结(Peyer’s patch)和肠系膜淋巴结。然而,这些转运途径并不能充分阐明口服LPS发挥生物学功能的机制。为了全面探究口服LPS的作用机制及其体内去向,关键在于建立检测体系,以评估给药后先天免疫细胞的状态。
口服LPS的研究展望
LPS是一种广泛存在的物质。例如,几乎所有食物中每克重量约含有1 ng至1 μg 的LPS。此外,人类口腔和肠道黏膜持续接触着大量的细菌。据估计,每克组织中的人体共生菌数量可达 10³ 至 10¹²(45)。因此,人类一生都持续暴露于LPS的环境中。有研究表明,这种LPS暴露方式可能对维持宿主免疫平衡(抗过敏倾向)(46, 47)以及肠道细菌感染防护具有重要作用(21)。
口服LPS的毒性极低,且已有大量研究提供有力证据,表明其对过敏性疾病及生活方式相关疾病具有多种益处。因此,在不久的将来,口服LPS有望被用于维持动物健康。为促进LPS的口服应用,需要阐明其预防和治疗各类疾病中的作用机制,但目前对口服LPS调控宿主健康的机制仍尚未明确。由于这些机制很可能与静脉注射LPS的作用方式截然不同,揭示其背后的原理显得尤为重要。
目前尚未开发出能够准确评估口服LPS反应的有效评估方法。我们认为,口服LPS的作用机制可归因于预激启动阶段的诱导(48)。在该阶段,先天免疫细胞对外源物质(细菌、病毒及凋亡细胞)的识别能力会上调。在小鼠模型中,静脉注射LPS(0.1-1 ng/只)即可诱导该启动阶段。该剂量约为LPS半数致死量(LD₅₀,200 μg/只)的二十万分之一(9),且不会引起小鼠血液中促炎细胞因子的释放,因此是安全无毒的。
预激阶段的分子标志之一,是巨噬细胞膜上存在 pro-TNF-α(49)。值得注意的是,pro-TNF-α 既可作为配体,也可作为受体,相互作用于相邻的巨噬细胞(即已被预激的巨噬细胞),并通过反向信号系统实现双向应答(50, 51)。综合这些数据,我们提出口服LPS维持体内平衡的机制,可能包括一种通过细胞间接触传递信号的系统(称为“巨噬细胞网络系统”)(26, 52)。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力