护肝成分卷了这么多年,这种"白色姜黄"为何在科研界脱颖而出?
白色姜黄&肝损伤防护
在快节奏的现代生活中,熬夜加班的咖啡、应酬桌上的酒、外卖盒里的重油重盐……我们的肝脏,每天都在默默承受着多重夹击,早已不堪重负。肝损伤,这一全球性的健康难题,正以逐年攀升的发病率,悄然威胁着无数人的生命质量。从酒精的侵蚀到药物的副作用,再到化学物质的伤害,肝损伤的成因复杂多样,后果却同样严峻——肝纤维化、肝硬化乃至肝癌,每一步都让人心惊胆战。数据显示,药物性肝损伤逐年攀升至全球第五大死因,酒精相关的肝病更是占据肝硬化致死病例的近三成……这场步步紧逼的肝脏危机,已成为现代人无法忽视的健康隐痛。
然而,在自然的馈赠中,我们或许能找到一线希望。姜黄素早已被熟知,而它的活性升级版——四氢姜黄素(因其呈白色也被称为“白色姜黄”Tetrahydrocurcumin, THC),正凭借更稳定、更易发挥作用的优势,走进科研视野。作为姜黄素的核心活性代谢产物,四氢姜黄素摒弃了普通姜黄素“难吸收”的短板,凭借更高的生物利用度,在实验室里展现出惊人潜力:在抗氧化、抗炎、抑制肝细胞凋亡等方面表现突出,可通过多条关键信号通路,减轻肝脏氧化应激与炎症反应,为肝损伤防护提供了全新思路。
多年来,全球科学家围绕这种“白色姜黄”发表了数百篇研究论文。这究竟是营销噱头,还是确有科学依据?我们梳理了国内外最新研究文献,带你一文读懂四氢姜黄素的护肝真相——不讲玄学,只说证据。今天,我们就结合最新研究进展,从权威研究出发,系统梳理四氢姜黄素的护肝功能、作用机制与研究进展,带你看懂这一成分到底有多“硬核”,也教你理性看待相关健康产品,科学守护肝脏健康。
四氢姜黄素抗肝损伤的研究进展
摘要
肝损伤已成为全球范围内严重的肝脏疾病,其发病率逐年上升,给各国人民带来沉重的健康负担。四氢姜黄素是姜黄素的活性代谢产物,具有抗氧化、抗炎、抑制细胞凋亡、抗肿瘤及抗衰老等药理作用。它能够通过MAPK、PI3K/Akt、PPAR、AMPK和Nrf2等信号通路,抑制肝损伤状态下肝细胞的凋亡,降低肝脏组织的氧化应激和炎症水平,从而达到预防和控制肝损伤的目的。本文通过查阅国内外文献,综述了四氢姜黄素的活性结构、药理作用及其在肝损伤中的应用,以期为四氢姜黄素在肝损伤领域的深入研究提供参考。
背景
肝损伤是指由一种或多种原因导致肝细胞损伤及肝脏生理结构改变,进而引发肝功能衰竭的病理反应。随着疾病的持续发展,可导致肝纤维化、肝硬化、肝细胞癌等严重疾病[1]。常见肝损伤类型包括酒精性肝损伤(ALI)、化学性肝损伤(CLI)和药物性肝损伤(DILI),其典型的病变特征包括肝细胞变性坏死、炎性细胞浸润、脂肪变性以及纤维组织形成[2, 3]。近年来,肝损伤的发病率持续上升。根据世界卫生组织统计数据,药物性肝损伤已上升为全球第五大死因;而全球疾病负担(GBD)数据显示,酒精相关肝损伤占肝硬化和慢性肝病致死病例的27%[4,5]。由于不同因素诱发肝损伤的内在机制尚未得到系统阐明,且肝损伤机制复杂,炎症、氧化应激、细胞凋亡和坏死是不同类型肝损伤的共同结果,涉及上游多靶点和多通路的共同作用[6]。因此,基于肝损伤复杂的发病机制及高发病率,阐明新的作用通路及其协同效应,并寻找适用于各类肝损伤的新型治疗药物,是当前亟待解决的问题。
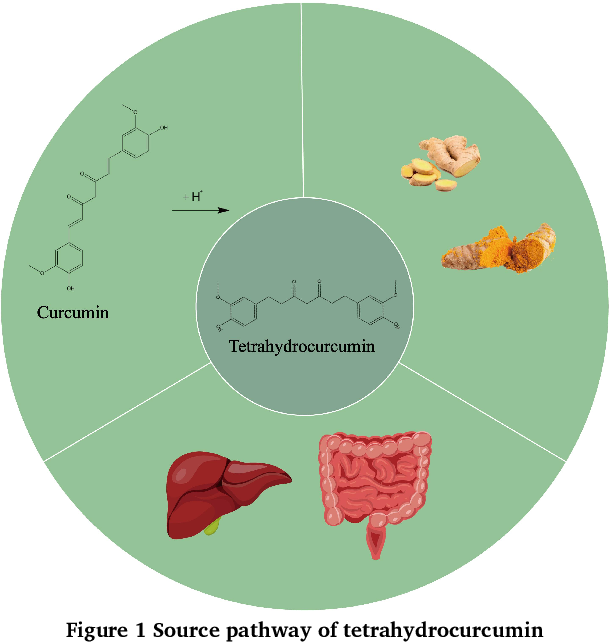
四氢姜黄素(THC)是姜黄素的活性代谢产物,最早由Holder等人在大鼠胆汁及代谢物中检测发现。该物质通过氢化还原反应在体外和体内由姜黄素转化衍生而来,或天然存在于姜属植物,包括蘘荷(Zingiber mioga)、姜(Z. officinale)和莪术(Curcuma zedoaria)等植物的根茎中(见图1)[7-11]。现代药理学研究表明,THC能够通过多靶点、多通路发挥抗氧化、抗炎及抑制细胞凋亡的作用,并在预防和控制肝损伤方面具有显著成效。本文综述了THC的活性结构、药理作用及其在肝损伤中的应用,旨在为后续深入研究提供参考依据。
图1 .四氢姜黄素的来源途径。
四氢姜黄素抗肝损伤的活性结构
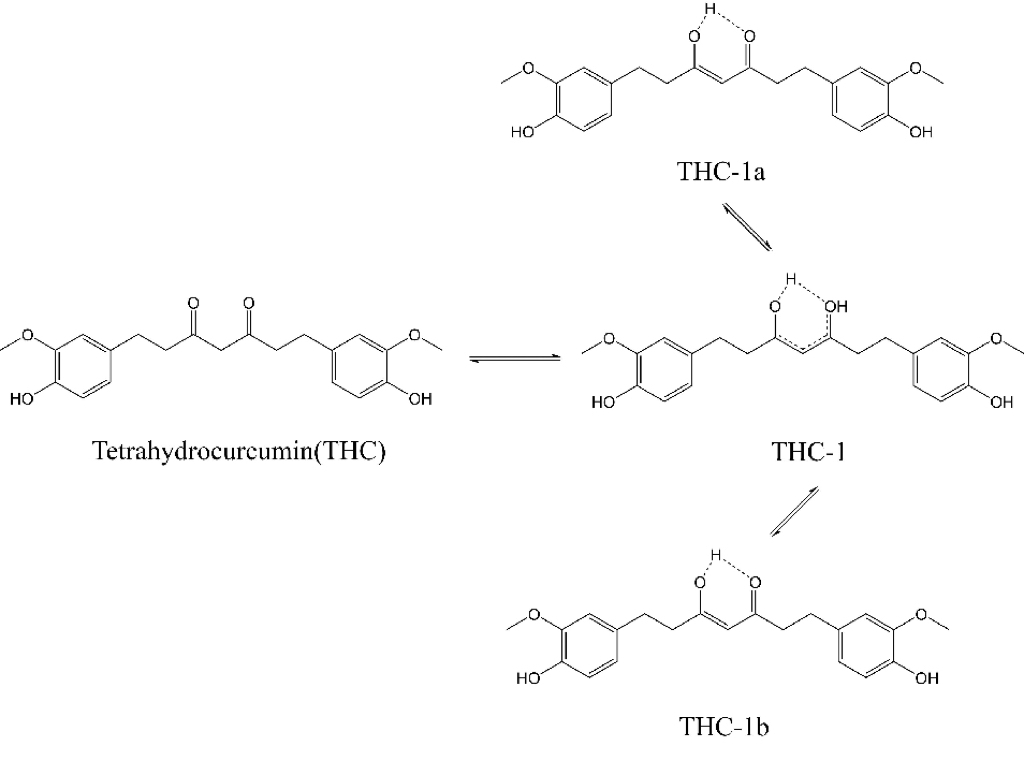
研究表明,当肝脏中活性氧自由基(ROS)与抗氧化能力之间的平衡被打破时,会引发肝脏氧化应激。乙醇及某些药物会导致肝脏ROS水平升高,进而诱发肝损伤,因此缓解氧化应激是改善肝损伤的重要策略之一[12]。四氢姜黄素(THC)结构中的β-二酮部分,通过断裂两个羰基之间活性亚甲基碳上的C-C键,展现出抗氧化活性[13]。姜黄素在体内代谢生成THC的过程中,其结构中心的共轭双链被氢化,这一变化显著增强了四氢姜黄素的抗氧化活性[14]。Trivedi等采用核磁共振(NMR)对溶液中的THC进行分析,首次发现THC在溶液中根据保留时间以三种互变异构形式存在:一种酮式结构和两种烯醇式结构(见图2)[15]。通过液相-质谱联用、气相色谱及光谱学技术对THC进行综合表征进一步证实,姜黄素在固态和液态中均以酮-烯醇形式存在,其中烯醇式为THC的稳定构型。这表明THC存在形式的改变可能是其抗氧化活性变化的原因之一。
图2.四氢姜黄素结构。
四氢姜黄素预防肝损伤的药理作用
抗氧化作用
在代谢性肝损伤中,脂质代谢紊乱导致的肝脏脂质蓄积会影响不同的ROS生成源,包括线粒体和内质网,从而破坏肝脏氧化与抗氧化能力的平衡[16]。而THC的抗氧化能力体现在其能够抑制体内ROS的产生,提高清除氧自由基的两种关键酶——超氧化物歧化酶(SOD)和谷胱甘肽过氧化物酶(GSH-Px)的表达,同时抑制氧化应激指标物丙二醛(MDA)的生成,这是减轻氧化应激对肝脏影响的有利因素。Li等在体外和体内实验中证实,THC可通过沉默信息调节因子1(SIRT1)抗氧化通路,显著抑制糖尿病诱导的ROS升高,从而发挥抗氧化作用[17]。其机制为:THC逆转糖尿病诱导的SIRT1表达降低,减少乙酰化SOD2(Ac-SOD2)表达并增强SOD2去乙酰化,以减少ROS生成;最终通过修复SOD和GSH-Px的活性、降低MDA的生成来增强自身的抗氧化能力。此外,THC还能上调抗氧化蛋白的表达,包括核因子红系相关因子2(Nrf2)和NAD(P)H苯醌氧化还原酶1(NQO1),减少体内ROS的蓄积[18]。ROS与脂质相互作用导致的脂质过氧化是氧化应激的另一种表现形式。Chaniad等比较了姜黄素及其衍生物对低密度脂蛋白(LDL)氧化的影响,结果显示在所测试化合物中对脂质和自由基的作用效果依次为:四氢姜黄素(THC) ≥ 姜黄素 ≥ 姜黄素类似物 > 去甲氧基姜黄素≥ 双去甲氧基姜黄素 ≥ 维生素E[19]。该结果表明THC具有更强的抗氧化活性,其作用机制可能通过抑制脂质过氧化及降低脂质氧化诱导的自由基增加来实现。
抗癌作用
在代谢应激性肝损伤中,非酒精性脂肪性肝病(NAFLD)患者可能出现不同程度的淋巴细胞亚群紊乱,其中白细胞介素IL-10/IL-17比例的失衡会促进肝细胞的炎症反应,导致肝损伤进一步加重。因此,抑制炎症反应是改善肝损伤治疗的重要方向之一[20]。机制研究表明,四氢姜黄素(THC)可通过丝裂原活化蛋白激酶磷酸酶(MAPK)信号通路和核因子-κB(NF-κB)信号通路有效抑制炎症反应中促炎因子和炎症因子的产生。具体机制为:THC通过上调丝裂原活化蛋白激酶磷酸酶1,阻止c-Jun氨基末端激酶(JNK)和细胞外信号调节蛋白激酶(ERK)的磷酸化,从而抑制肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)和白细胞介素-6(IL-6)的释放[18]。NF-κB信号通路是经典的炎症通路,THC通过调控NF-κB进而影响其下游靶点如TNF-α和IL-1β的表达水平,有效缓解炎症反应[21]。在采用四氢姜黄素(THC)干预脂多糖刺激的RAW264.7巨噬细胞氧化应激和炎症反应的实验中,发现THC能显著抑制一氧化氮(NO)、NF-κB的产生和活化,并降低MAPK和ERK的磷酸化,表明THC可能通过NF-κB/MAPK通路在炎症反应中发挥有益作用,特别是在本实验中THC表现出比姜黄素更强的抗炎活性[22]。Koh等人在经THC给药的小鼠粪便中鉴定出代谢产物3-氨基-3-脱氧四氢姜黄素(THC-NH2),其抗炎活性显著优于前者[23]。在THC-NH2存在条件下,一氧化氮合酶(iNOS)蛋白表达水平显著降低,在亚硝酸盐生成方面发挥显著的抗炎效应,但不会增加前列腺素E2的水平。
抑制细胞凋亡
细胞凋亡是一种程序性细胞死亡的主动模式,肝组织细胞的过度凋亡是肝损伤发生发展的重要因素。实验发现,药物诱导的肝细胞凋亡通路激活、坏死性凋亡、自噬和细胞焦亡是药物性肝损伤的常见模式,而抑制肝细胞凋亡有助于改善肝损伤[24,25]。Chen等研究发现,,四氢姜黄素(THC)能有效降低凋亡相关蛋白(如B细胞淋巴瘤相关X蛋白(Bax)、半胱氨酸蛋白酶-3(caspase-3))的表达,并上调了Bcl-2蛋白的表达;逆转了缺氧/复氧诱导的磷脂酰肌醇3-激酶(PI3K)、苏氨酸蛋白激酶(Akt)和哺乳动物雷帕霉素靶蛋白(mTOR)磷酸化水平的下降,并诱导缺氧诱导因子-1α(HIF-1α)表达[26]。从而基于PI3K/AKT/mTOR通路,有效预防心肌细胞凋亡。除此之外,THC还能通过Ras/ERK信号通路抑制小胶质细胞的细胞周期阻滞和凋亡。在阿尔茨海默病小鼠模型中,THC上调转化生长因子β1(TGF - β1)和Bag1的表达,并减弱Gab2、Ccnd2、K-Ras、多聚ADP核糖聚合酶1(PARP1)、caspase-3和TNF-α的异常表达。其中Bag1是一种多功能抗凋亡蛋白,而Gab2和Ccnd2与细胞异常增殖相关[27]。THC能有效恢复谷氨酸诱导的神经元凋亡。染色质凝聚是凋亡的形态学特征,THC可有效阻止谷氨酸诱导的HT22细胞染色质凝聚。在碘化丙啶(PI)和膜联蛋白V(Annexin V)染色观察下,发现THC能显著减少谷氨酸诱导的HT22细胞凋亡[28]。
四氢姜黄素在肝损伤中的作用
非酒精性脂肪性肝病
非酒精性脂肪性肝病(NAFLD)是一种代谢应激性肝损伤,包括单纯性非酒精性脂肪肝(NAFL)——由脂肪过度蓄积发展而来,以及非酒精性脂肪性肝炎(NASH)——以门静脉和小叶炎症及肝细胞损伤为特征[29,30]。在一项研究中,Gao等人通过实验发现,THC可通过改善脂质代谢和氧化还原稳态来预防非酒精性脂肪性肝病(NAFLD)[31]。THC降低了NAFLD小鼠肝脏中成纤维细胞生长因子21(FGF21)的表达,并上调细胞色素450 51(CYP51)和FOXQ1的mRNA水平,从而调节小鼠的糖脂代谢和氧化应激。在细胞实验中,经油酸(OA)处理的HepG2细胞在THC干预后,细胞内NRF2及其靶基因NQO1、GSTA1、GCLM和GCLC的表达均随THC剂量增加而升高,且THC显著提高了HepG2细胞中FGF21 mRNA的表达。该研究表明,THC改善了高脂饮食诱导的体重增加、血脂和血糖升高以及肝脏脂肪变性等病理改变。有趣的是,THC既未影响也未降低NAFLD小鼠的体重,同时未改变其摄食量,这一现象可能与THC对FGF21的刺激作用有关。FGF21本身不影响摄食量,但能显著增加特定刺激下的能量消耗,从而避免体重增加。此外,这可能与FGF21具有抗肥胖特性有关[32,33]。FGF21具有维持能量稳态的生理功能,THC通过刺激FGF21的表达降低外周胰岛素抵抗,减少脂肪生成和糖异生的底物通量,并间接影响肝脏糖脂代谢,从而达到改善NAFLD的效果[34,35]。在另一项细胞实验中,Chen等人使用不同浓度的THC处理油酸(OA)诱导的NAFLD细胞模型[36]。研究发现,THC通过抑制脂肪生成蛋白——固醇调节元件结合蛋白1(SREBP-1c)、过氧化物酶体增殖物激活受体γ(PPARγ)、脂肪酸合酶(FAS)和脂肪酸结合蛋白4(FABP4)的表达,减少HepG2细胞的脂质蓄积;此外,THC以腺苷酸激活蛋白激酶(AMPK)依赖性方式减轻了OA诱导的肝脏脂肪生成。在葡萄糖摄取和胰岛素抵抗方面,THC通过胰岛素受体底物1(IRS-1)/PI3K/Akt及其下游信号通路FOXO1和糖原合酶3β(GSK3β)的磷酸化,恢复了OA培养的HepG2细胞的葡萄糖摄取和胰岛素信号传导。该实验结果阐明了THC改善肝脏脂肪变性的机制,并证实THC通过减少脂质生成和蓄积、增强胰岛素信号传导,对改善NAFLD有益。在最新的研究实验中,Wu等人通过体内外实验发现,姜黄素可通过NF-κB和PI3K/Akt/HIF-1α通路改善NASH大鼠的肝脏脂质蓄积、炎症和内皮功能障碍,且这一过程与姜黄素转化为THC密切相关;并在体外实验中证实THC改善NASH内皮功能障碍的效果强于姜黄素。深入研究发现,THC能显著提高一氧化氮(NO)水平,抑制ANGPT2表达,降低VCAM-1和细胞间黏附分子-1(ICAM-1)的mRNA水平,从而恢复肝窦内皮细胞(LSECs)的内皮功能;减轻核pp65/组蛋白H3、p-Akt/Akt和p-PI3K/PI3K比值的升高,并通过NF-κB和PI3K/Akt信号通路改善NASH细胞的内皮功能[37]。通过Akt信号通路改善NASH大鼠的肝脏状况。
酒精性肝损伤
酒精性肝病(ALD),又称酒精性肝病,包括单纯性脂肪变性、酒精性肝炎(AH)、肝硬化以及叠加的肝细胞癌,其主要致病机制为氧化应激、炎症反应和肝细胞凋亡[38, 39]。发酵姜黄能有效抑制酒精性脂肪肝小鼠体内CYP2E1和SREBP-1c蛋白的表达,提高PPAR-α水平,增加AMPK和CPT-1的表达,并降低ACC的表达,从而分别减少脂肪酸合成、促进脂肪酸氧化,在一定程度上改善酒精性脂肪肝;经高效液相色谱法(HPLC)分析发现,其中THC和咖啡酸含量高于生姜黄,表明THC含量的增加可能在预防酒精性脂肪肝中发挥作用[40]。SREBP-1c是脂质稳态的主要调节因子,PPAR-α是胆固醇生成和代谢的重要环节,已有实验证实THC可作用于非酒精性脂肪肝(NAFLD)并显著影响SREBP-1c蛋白和PPAR-α的表达,而发酵姜黄中THC含量的增加可能是增强其对SREBP-1c蛋白和PPAR-α作用效果的关键,从而在一定程度上改善酒精性肝病(ALD)[41, 42]。
药物性肝损伤
药物性肝损伤(DILI)是指由各类药物、膳食补充剂甚至辅料引发的肝脏损伤。非甾体抗炎药(NSAIDs)是导致肝损伤最常见的诱因,在常规剂量使用下约10%的患者会出现不同程度的肝损伤[43]。对乙酰氨基酚(APAP)是一种广泛使用的具有解热镇痛作用的非甾体抗炎药,通常用于退热和止痛。APAP大部分(85%)经肝脏代谢后通过尿液和胆汁排出,但少量(15%)经CYP450酶代谢会产生具有毒性的NAPQI,从而导致肝损伤[44]。过量使用APAP容易引发急性药物性肝损伤和急性肝衰竭[45]。Luo等人采用APAP诱导小鼠肝损伤模型,经THC干预后,小鼠受损的肝功能和肝脏抗氧化状态得到恢复,脂质过氧化标志物水平显著降低,表现出强效的抗氧化和肝保护作用[46]。在该实验中,THC在有效浓度范围内呈剂量依赖性增强肝功能并减轻肝损伤病理改变,通过提高GSH、SOD、CAT和T-AOC水平恢复肝脏抗氧化能力,显著抑制CYP2E1活性及其表达,并大幅增强Nrf2靶向基因(GCLC、GCLM、NQO1和HO-1)的转录活性,THC通过降低肝脏氧化应激水平改善APAP诱导的药物性肝损伤。CYP2E1是肝脏中主要的活性氧(ROS)产生源之一,THC可通过影响CYPs减少ROS和自由基的生成,从而降低氧化应激水平,减轻肝脏损伤[47,48]。值得注意的是,在改善红霉素酯诱导的肝损伤方面,THC表现出优于水飞蓟素的肝保护效果[49]。
中毒性肝损伤
在工业生产中,人们通过职业或环境因素接触重金属(如镉(Cd)、砷(As)等)的概率较高。当这些重金属在肝脏、肾脏等器官中蓄积,超过一定阈值后会引发一系列疾病[50]。动物实验已证实,THC能有效改善Cd和As诱导的肝毒性,恢复受损的肝功能和肝脏抗氧化状态,并显著降低脂质过氧化标志物水平,表现出强效的抗氧化和护肝作用[51, 52]。
结论
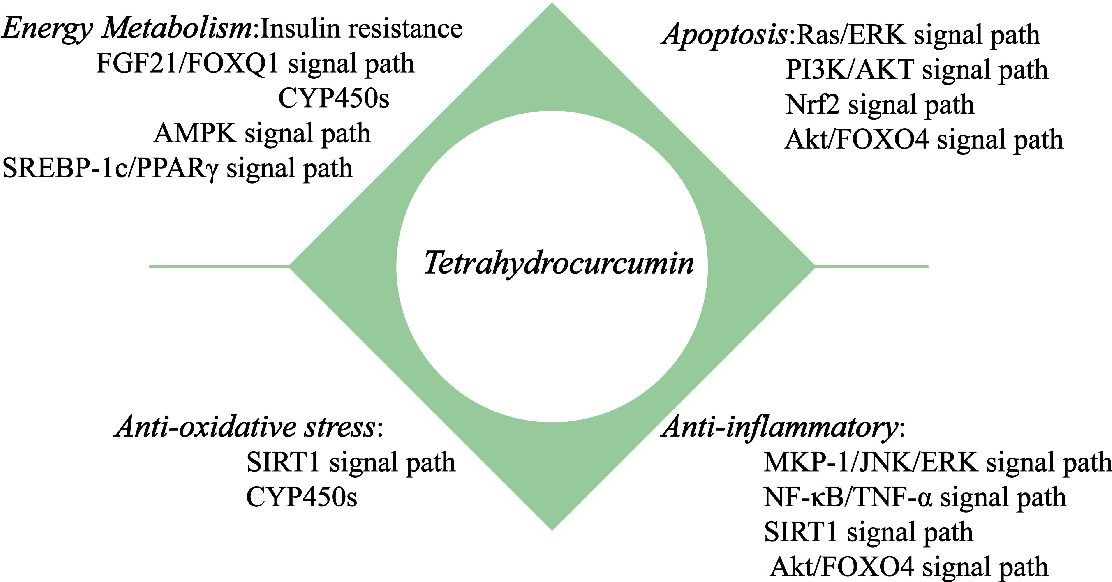
四氢姜黄素具有广泛的药理作用(见图3),在肝脏、心血管、脑部及其他器官相关疾病的研究中已取得一定成果。这可能归因于四氢姜黄素作为姜黄素的活性代谢产物,仍存在水溶性差、生物利用度低等问题。但随着研究的深入,新工艺方法可有效解决此类问题,为四氢姜黄素在肝损伤及其他疾病中的作用机制研究提供支持,从而使其展现出更大的开发潜力。肝损伤涵盖多种疾病,其发病机制复杂,除氧化应激、炎症、细胞凋亡等生理变化外,还涉及糖脂代谢紊乱、肠道微生物、肝代谢酶及肝组织纤维化等因素的影响。目前国内外研究均表明,四氢姜黄素与这些生理变化或作用通路密切相关,这为后续从多角度、多层面深入研究四氢姜黄素改善肝损伤的作用机制提供了参考和方向。
图3.四氢姜黄素在肝损伤中的作用机制。
关于四氢姜黄素补充剂:
目前,以四氢姜黄素(THC)为主要成分的膳食补充剂在市面上尚不多见。但随着相关研究的不断深入,未来这类产品有望逐步进入消费市场。
如果您在选购时遇到宣称含有“四氢姜黄素”的营养品,可参考以下原则进行理性判断:
- 看含量:关注产品中四氢姜黄素的实际含量与标注是否清晰、透明;
- 看配方:留意是否添加了有助于吸收或协同增效的辅料成分;
- 看品牌信誉:优先选择具备科研背景、质量认证和良好口碑的品牌。
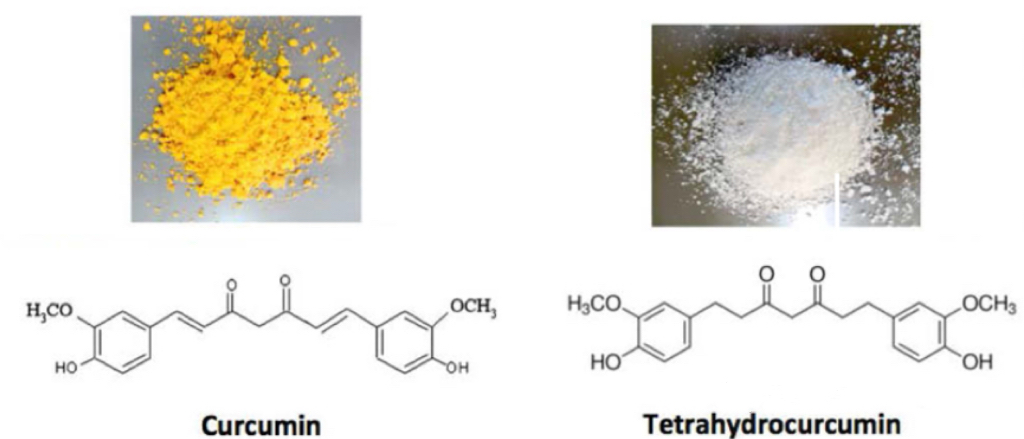
值得注意的是,四氢姜黄素本身为白色、无味的粉末状物质,适合开发为口服液、粉剂、胶囊等多种剂型。未来上市时,产品可能以“白姜黄素”“四氢姜黄素提取物”等名称标示,建议消费者在选购时多加留意。对于新型原料产品,尤其应关注厂商是否提供可靠的科研依据与权威的质量认证,以确保其功效与安全性具备实质支撑。
最后,牢记理性看待姜黄素类补充剂的定位——它不是“万能药”,更不能替代医生处方的正规治疗。在选购和服用过程中,如出现任何不适症状,应及时停止使用并咨询专业人士。按照推荐剂量服用,一般姜黄素补充剂是安全的;但若过量使用,也可能引起胃肠不适(如腹泻、恶心)等反应。唯有科学选择、品质保障,再配合健康的生活方式,才能真正发挥此类成分对身体的积极作用。
免责声明:
以上部分内容来源于外网我们重在信息分享,版权归属原作者或原刊发平台所有,如有侵权、信息有误或其他异议,请联系处理,我们将在24小时内删除或整改。
复合免疫 健康活力